题目内容
17.某气体是由SO2、H2、CO2中的一种或几种组成,现测知气体里含氧的质量分数为50%,则该气体中的组成可能有SO2、H2、CO2、SO2、H2、CO2.分析 本题探究物质的组成要利用元素质量分数的计算,在SO2中氧元素的质量分数为$\frac{16×2}{32+16×2}×100%$=50%,若是一种气体,应是SO2.
在CO2中氧元素的质量分数为$\frac{16×2}{12+16×2}×100%$=72.7%>50%,若有CO2存在,必须有不含氧元素的气体存在或氧元素的质量分数小于50%,即可能是H2、CO2或SO2、H2、CO2
解答 解:SO2中氧元素的质量分数为$\frac{16×2}{32+16×2}×100%$=50%,CO2中氧元素的质量分数为$\frac{16×2}{12+16×2}×100%$=72.7%,所以若是一种气体,应为SO2
若是混合气体,要满足氧元素的质量分数为50%
则必须有不含氧元素的气体存在或氧元素的质量分数小于50%,即可能是H2、CO2或SO2、H2、CO2
故答案为:①SO2②H2、CO2③SO2、H2、CO2.
点评 此题关键是将三种物质相互间混合,寻找氧元素的质量分数可能是50%的.本题难度较大,考查混合物中某元素的质量分数的计算.

练习册系列答案
相关题目
18.通过化学学习,我们了解了生活中物质变化的本质.下列变化中与其它不同的是( )
| A. | 木柴劈成块 | B. | 西瓜榨成汁 | C. | 海水晒盐 | D. | 米饭变馊 |
19.下列物质鉴别的实验方法错误的是( )
| 选项 | 鉴别的物质 | 实验方法及现象 |
| A | 铁和锌 | 滴加稀盐酸,观察是否产生气泡 |
| B | 食盐和纯碱 | 滴加食醋,观察是否产生气泡 |
| C | 过氧化氢和蒸馏水 | 加入二氧化锰,观察是否产生气泡 |
| D | 碳酸氢铵和硫酸铵 | 滴加稀盐酸,观察是否产生气泡 |
| A. | A | B. | B | C. | C | D. | D |
2. 2012年1月15日,广西龙江河发生镉污染事件,如图是镉元素在元素周期表中的信息,从该图获取的信息中,正确的是( )
2012年1月15日,广西龙江河发生镉污染事件,如图是镉元素在元素周期表中的信息,从该图获取的信息中,正确的是( )
 2012年1月15日,广西龙江河发生镉污染事件,如图是镉元素在元素周期表中的信息,从该图获取的信息中,正确的是( )
2012年1月15日,广西龙江河发生镉污染事件,如图是镉元素在元素周期表中的信息,从该图获取的信息中,正确的是( )| A. | 镉原子的核外有48个电子 | B. | 镉元素的原子序数为112 | ||
| C. | 镉元素属于非金属元素 | D. | 镉元素相对原子质量为112.4g |

 ”表示一个氢原子,则“
”表示一个氢原子,则“ ”表示H2(填写物质化学式),从图2中可知,汞的核电荷数是80;
”表示H2(填写物质化学式),从图2中可知,汞的核电荷数是80;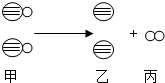 通过如图微观模拟化学反应示意图回答下列问题.
通过如图微观模拟化学反应示意图回答下列问题.