题目内容
14.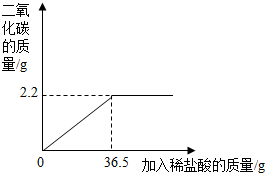 某星期日,石门中学初三(二)班化学兴趣小组的同学到石家庄市西郊的山上采集到一种石灰石,带回学校后,在实验室里进行如下实验:取样品10g放入试管中,向试管里逐滴滴入稀盐酸,当不再有气体产生时,恰好用去稀盐酸36.5g.其反应进程如图所示.
某星期日,石门中学初三(二)班化学兴趣小组的同学到石家庄市西郊的山上采集到一种石灰石,带回学校后,在实验室里进行如下实验:取样品10g放入试管中,向试管里逐滴滴入稀盐酸,当不再有气体产生时,恰好用去稀盐酸36.5g.其反应进程如图所示.请计算:
(1)请计算所加入的稀盐酸的溶质质量分数.
(2)同学们所采集的石灰石中含碳酸钙的质量分数.
分析 (1)由图可知生成二氧化碳的质量,利用二氧化碳的质量求出稀盐酸的溶质质量分数即可;
(2)由二氧化碳和样品的质量根据碳酸钙与稀盐酸反应的化学方程式可以计算出样品中碳酸钙的质量分数即可.
解答 解:(1)由图中曲线可知生成二氧化碳的质量为2.2g.
设样品中碳酸钙的质量为x,稀盐酸的溶质质量为y.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73 44
x y 2.2g
$\frac{100}{x}=\frac{73}{y}=\frac{44}{2.2g}$
解得:x=5g
y=3.65g
所加入的稀盐酸的溶质质量分数=$\frac{3.65g}{36.5g}×100%$=10%.
(2)所采集的石灰石中含碳酸钙的质量分数=$\frac{5g}{10g}×100%$=50%
答:(1)所加入的稀盐酸的溶质质量分数为10%.
(2)所采集的石灰石中含碳酸钙的质量分数位50%.
点评 此题考查的根据关化学方程式的计算,通过认真分析题干,直接得到二氧化碳的质量,然后再求碳酸钙的质量.

练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案
相关题目
4.实验室制取二氧化碳,常用的药品是( )
| A. | 大理石和稀盐酸 | B. | 锌和稀硫酸 | ||
| C. | 氯酸钾和二氧化锰 | D. | 高锰酸钾 |
2.对于下列几种化学符号,有关说法正确的是( )
①N ②Na+③ ④P2O5⑤KClO3.
④P2O5⑤KClO3.
①N ②Na+③
 ④P2O5⑤KClO3.
④P2O5⑤KClO3.| A. | 表示物质组成的化学式有①④⑤ | |
| B. | 表示阳离子的有②③ | |
| C. | ④中数字“5”表示五氧化二磷中有5个氧原子 | |
| D. | ⑤中氯元素的化合价为+5价 |
6.下列物质中属于纯净物的是( )
| A. | 天然气 | B. | 工业酒精 | C. | 干冰 | D. | 加铁酱油 |
3.2000年度诺贝尔化学奖授予了开辟“导电塑料”领域的三位科学家,在其相关技术中用碘(I2)来掺杂塑料,能使其导电能力增加10倍.碘(I2)属于( )
| A. | 非金属单质 | B. | 金属单质 | C. | 化合物 | D. | 混合物 |
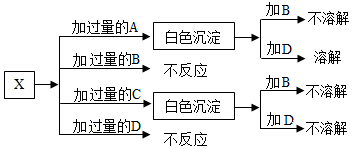 A、B、C、D分别是NaNO3、NaOH、HNO3和Ba(NO3)2四种物质的溶液,现利用一种可溶性镁盐X做如图所示的实验,就可将它们一一鉴别出来:
A、B、C、D分别是NaNO3、NaOH、HNO3和Ba(NO3)2四种物质的溶液,现利用一种可溶性镁盐X做如图所示的实验,就可将它们一一鉴别出来: 某元素的离子对维持人体细胞内外正常的水分分布和促进细胞内外物质交换起主要作用.该元素的离子带一个单位正电荷,其结构示意图为则n=19,原子有4个电子层,此元素属于金属(填“金属”、“非金属”)元素.
某元素的离子对维持人体细胞内外正常的水分分布和促进细胞内外物质交换起主要作用.该元素的离子带一个单位正电荷,其结构示意图为则n=19,原子有4个电子层,此元素属于金属(填“金属”、“非金属”)元素.