题目内容
1.73g质量分数为20%的盐酸与足量的大理石反应,生成二氧化碳的质量是多少?分析 大理石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳,根据盐酸的质量、溶质质量分数可以计算生成二氧化碳的质量.
解答 解:设生成二氧化碳的质量为x,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
73 44
73g×20% x
$\frac{73}{73g×20%}$=$\frac{44}{x}$,
x=8.8g,
答:生成了8.8g二氧化碳.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.某课外活动小组为测定某不纯锌粒中含锌的质量分数,取来了一些锌粒样品,并取稀硫酸800g,平均分成4份,将四份不同质量的样品加入到四份稀硫酸中,进行实验(杂质不与稀硫酸反应),结果如下:
?(1)上表中m的数值是0.40;
?(2)试计算这种锌粒样品中锌的质量分数(写出计算过程).
| 实验 | 1 | 2 | 3 | 4 |
| 加入样品是质量/g | 6.5 | 13 | 19.5 | 26 |
| 生成H2的质量/g | 0.16 | 0.32 | 0.40 | m |
?(2)试计算这种锌粒样品中锌的质量分数(写出计算过程).
9.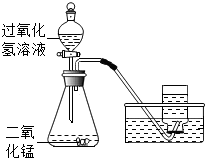 某同学在实验室用溶质质量分数为10%过氧化氢溶液和二氧化锰制取氧气,恰好完全反应,实验的相关数据如下表.
某同学在实验室用溶质质量分数为10%过氧化氢溶液和二氧化锰制取氧气,恰好完全反应,实验的相关数据如下表.
(1)反应生成氧气的质量为1.6g;
(2)计算原混合物中二氧化锰的质量,并写出必要的计算过程.
 某同学在实验室用溶质质量分数为10%过氧化氢溶液和二氧化锰制取氧气,恰好完全反应,实验的相关数据如下表.
某同学在实验室用溶质质量分数为10%过氧化氢溶液和二氧化锰制取氧气,恰好完全反应,实验的相关数据如下表.| 发生装置内物质的总质量 | |
| 反应前 | 34.3g |
| 反应后 | 32.7g |
(2)计算原混合物中二氧化锰的质量,并写出必要的计算过程.
16. 如图是A、B、C三种固体物质的溶解度曲线,下列分析不正确的是( )
如图是A、B、C三种固体物质的溶解度曲线,下列分析不正确的是( )
 如图是A、B、C三种固体物质的溶解度曲线,下列分析不正确的是( )
如图是A、B、C三种固体物质的溶解度曲线,下列分析不正确的是( )| A. | 20℃时,三种物质的溶解度由大到小的顺序是B>A=C | |
| B. | 50℃时,把50g A放入50 g水中能形成100g A的饱和溶液 | |
| C. | 将C的饱和溶液变为不饱和溶液,可采用降温或加水的方法 | |
| D. | 分别将三种物质的饱和溶液从50℃降至20℃时,所得溶液溶质质量分数大小关系是B>A>C |
6.下列说法正确的是( )
| A. | 发明一种催化剂可以到达“水变油”的目的 | |
| B. | 常温下pH小于3的溶液能使紫色石蕊溶液变红 | |
| C. | 稀释浓硫酸的正确方法是将水沿玻璃棒注入浓硫酸中 | |
| D. | 碳酸氢钙、淀粉、金刚石、维生素、蛋白质都属于有机物 |
13.区别下列各组物质,所选择试剂和方法错误的是( )
| A. | 羊毛和涤纶(点燃后闻气味) | B. | 硬水和软水(肥皂水) | ||
| C. | 火碱溶液和石灰水(CO2) | D. | 烧碱溶液和食盐水(CO2) |
