题目内容
11.请回答下列与浓硫酸、氢氧化钠和生石灰有关的问题.(1)要把50g98%的浓硫酸稀稀为质量分数为20%的硫酸,需要水的质量是195g;
(2)氢氧化钠敞口放置会潮解,说明氢氧化钠具有吸水性;
(3)在H2、O2、CO、CO2、NH3五种气体中,不能用于生石灰干燥的是CO2.
分析 (1)加水稀释可以把浓溶液变成稀溶液,溶液稀释前后,溶质的质量不变,据此回答问题即可;
(2)根据氢氧化钠的性质解答;
(3)根据干燥的物质不能与干燥剂发生反应解答.
解答 解:(1)设稀释后溶液的质量为x
根据溶液稀释前后溶质的质量不变,
50g×98%=x×20%
x=245g
需要水的质量是:245g-50g=195g
答:需要水195g.
(2)氢氧化钠具有吸水性,敞口放置会潮解;故填:吸水
(3)氧气、氢气和氨气等气体不能与生石灰反应,可以使用生石灰做干燥剂,故填:CO2
点评 本题考查了常见的物质干燥剂,完成此题,可以依据物质的性质进行.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案
相关题目
2.下列现象中,一定发生化学变化的是( )
| A. | 木材燃烧 | B. | 汽油挥发 | C. | 干冰升华 | D. | 石蜡熔化 |
6.下列说法中,正确的是( )
| A. | CH4和CO都能在空气中燃烧,所以都可以用作燃料 | |
| B. | 铜在金属活动性顺序表中排在氢后,所以氧化铜不能与稀盐酸发生反应 | |
| C. | 有机物都含有碳元素,所以含碳元素的化合物都属于有机物 | |
| D. | 向某无色溶液中加入酚酞溶液后酚酞变红色,说明该无色溶液一定是碱溶液 |
3.水是重要的资源.下列关于水的说法中,正确的是( )
| A. | 水是一种单质 | |
| B. | 过滤可除去污水中的不溶物,使污水变为纯水 | |
| C. | 净化水时,可用活性炭作杀菌剂 | |
| D. | 用肥皂水可区分硬水和软水 |
20.四氧化三铁可用于医疗器械、电子等工业.某实验兴趣小组从工厂采集废液(含FeSO4和少量ZnSO4、MgSO4),进行四氧化三铁的制备实验.
【阅读资料】
(1)25℃时,氢氧化物沉淀的pH范围如表.
(2)25℃时,Zn(OH)2可溶于pH>10.5的碱溶液.
(3)制备Fe3O4的实验流程如图:
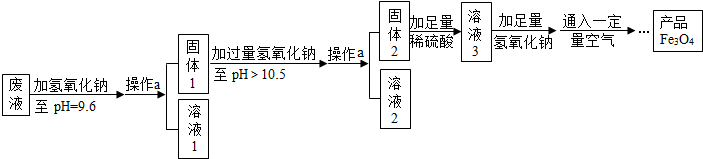
【回答问题】
(1)往废液中加入氢氧化钠溶液生成沉淀的化学方程式为(写一个即可)2NaOH+ZnSO4═Zn(OH)2↓+Na2SO4【或2NaOH+FeSO4═Fe(OH)2↓+Na2SO4】.
(2)溶液1所含溶质有(至少写两种)硫酸镁、硫酸钠;溶液3所含溶质的主要成分为硫酸亚铁.
(3)该实验取废液100g,最终得到产品四氧化三铁质量为2.32g,则原废液中硫酸亚铁溶质的质量分数不低于4.56%(精确到0.01%).
【阅读资料】
(1)25℃时,氢氧化物沉淀的pH范围如表.
| Zn(OH)2 | Fe(OH)2 | Mg(OH)2 | |
| 开始沉淀的pH | 5.7 | 7.6 | 10.4 |
| 沉淀完全的pH | 8.0 | 9.6 | 12.4 |
(3)制备Fe3O4的实验流程如图:

【回答问题】
(1)往废液中加入氢氧化钠溶液生成沉淀的化学方程式为(写一个即可)2NaOH+ZnSO4═Zn(OH)2↓+Na2SO4【或2NaOH+FeSO4═Fe(OH)2↓+Na2SO4】.
(2)溶液1所含溶质有(至少写两种)硫酸镁、硫酸钠;溶液3所含溶质的主要成分为硫酸亚铁.
(3)该实验取废液100g,最终得到产品四氧化三铁质量为2.32g,则原废液中硫酸亚铁溶质的质量分数不低于4.56%(精确到0.01%).
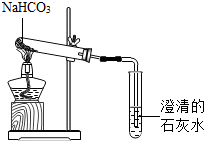 用如图所示装置加热NaHCO3,试管中留下的白色固体只有Na2CO3,并观察到试管内壁有水珠生成,澄清石灰水变浑浊.根据实验回答问题.
用如图所示装置加热NaHCO3,试管中留下的白色固体只有Na2CO3,并观察到试管内壁有水珠生成,澄清石灰水变浑浊.根据实验回答问题.