题目内容
11.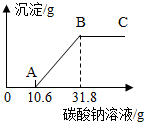 在做完“用稀盐酸和石灰石反应制取二氧化碳”的实验后,小明突然想到:是否可以测得实验所用的石灰石中碳酸钙的含量呢?小明又进行了如下实验:①将试管中反应的剩余物过滤并多次用蒸馏水洗涤,得到滤液和滤渣.②向滤渣中滴加稀盐酸,无明显的现象.③将滤渣干燥后称量,质量为0.5g.④向滤液中加入10%的Na2CO3溶液,获得了相关的数据,并绘制成如图所示的图象.根据小明的实验过程回答下列问题.(假设石灰石中的其余杂质不与稀盐酸反应)
在做完“用稀盐酸和石灰石反应制取二氧化碳”的实验后,小明突然想到:是否可以测得实验所用的石灰石中碳酸钙的含量呢?小明又进行了如下实验:①将试管中反应的剩余物过滤并多次用蒸馏水洗涤,得到滤液和滤渣.②向滤渣中滴加稀盐酸,无明显的现象.③将滤渣干燥后称量,质量为0.5g.④向滤液中加入10%的Na2CO3溶液,获得了相关的数据,并绘制成如图所示的图象.根据小明的实验过程回答下列问题.(假设石灰石中的其余杂质不与稀盐酸反应)(1)第②步中小明向滤渣中加入稀盐酸的目的是为了检验滤渣中是否还有剩余的CaCO3.
(2)第①步中如果在过滤时没有用蒸馏水多次洗涤,则测得碳酸钙的含量将偏小.(选填“偏大”、“不变”或“偏小”)
(3)根据图象及相关的数据可求得石灰石中碳酸钙的含量为多少?
分析 (1)根据碳酸钙难溶于水,而盐酸和碳酸钙反应生成二氧化碳气体进行解答;
(2)根据第①步中如果在过滤时没有用蒸馏水多次洗涤,则会造成碳酸钙的质量减小进行解答;
(3)根据从第10.6g开始碳酸钠溶液与氯化钙反应生成碳酸钙沉淀和氯化钠,生成碳酸钙的质量等于原来石灰石中碳酸钙的质量进行解答.
解答 解:(1)碳酸钙难溶于水,而盐酸和碳酸钙反应生成二氧化碳气体,向滤渣中滴加稀盐酸,无明显的现象,说明滤渣中没有碳酸钙,所以第②步中小明向滤渣中加入稀盐酸的目的是为了检验滤渣中是否还有剩余的CaCO3;故填:检验滤渣中是否还有剩余的CaCO3;
(2)第①步中如果在过滤时没有用蒸馏水多次洗涤,则会造成碳酸钙的质量减小,所以测得碳酸钙的质量分将偏小;故填:偏小;
(3)设碳酸钙的质量为x,
Na2CO3+CaCl2═2NaCl+CaCO3↓
106 100
(31.8g-10.6g)×10% x
$\frac{106}{(31.8g-10.6g)×10%}$=$\frac{100}{x}$
x=2g
石灰石中碳酸钙的含量为$\frac{2g}{2g+0.5g}$×00%=80%;
(1)检验滤渣中是否还有剩余的CaCO3
(2)偏小
(3)80%
点评 在解此类题时,首先分析题中考查的问题,然后结合学过的知识和题中的知识进行分析解答.

练习册系列答案
相关题目
6. 如图所示为向一定量某固体中逐滴加入某溶液至过量.若x轴表示加入溶液的质量,则y轴表示的含义正确的是( )
如图所示为向一定量某固体中逐滴加入某溶液至过量.若x轴表示加入溶液的质量,则y轴表示的含义正确的是( )
 如图所示为向一定量某固体中逐滴加入某溶液至过量.若x轴表示加入溶液的质量,则y轴表示的含义正确的是( )
如图所示为向一定量某固体中逐滴加入某溶液至过量.若x轴表示加入溶液的质量,则y轴表示的含义正确的是( )| 选项 | 固体 | 溶液 | y |
| A | 二氧化锰 | 过氧化氢溶液 | 水的质量 |
| B | 氢氧化钠和碳酸钠粉末 | 稀盐酸 | 二氧化碳体积 |
| C | 硫酸钡和碳酸钡混合物 | 稀硝酸 | 不溶固体质量 |
| D | 铁和铜的混合粉末 | 硫酸铜溶液 | 混合物中铜的质量 |
| A. | A | B. | B | C. | C | D. | D |
1.火电厂进的是“煤”,出的是“电”,在这个过程中能量的转化过程是( )
| A. | 化学能→内能→机械能→电能 | B. | 化学能→重力势能→动能→电能 | ||
| C. | 内能→化学能→机械能→电能 | D. | 机械能→内能→化学能→电能 |

 如图是空气中氧气含量的测定装置.试回答:
如图是空气中氧气含量的测定装置.试回答: