题目内容
5.在60℃时将36g硝酸钾溶于204g水中,将此溶液平均分成三等份:(1)取第一份,将温度升高到90℃,此时溶质的质量分数为15%.
(2)取第二份,要使其溶质的质量分数比原来增加一倍,需加入硝酸钾固体17.1g.
(3)取第三份,使其溶质的质量分数变为原来的一半,需加水80g.
分析 根据溶质的质量分数=$\frac{溶质质量}{溶液质量}×$100%,溶液具有均一性,进行分析解答.
(1)取第一份,将温度升高到90℃,溶液的组成未发生改变,进行分析解答.
(2)取第二份,要使其溶质的质量分数比原来增加一倍,结合溶质质量=溶液质量×溶质的质量分数,进行分析解答.
(3)根据溶液稀释前后溶质的质量不变,进行分析解答.
解答 解:溶质的质量分数=$\frac{溶质质量}{溶液质量}×$100%,在60℃时将36g硝酸钾溶于204g水中,所得溶液中溶质质量分数为$\frac{36g}{36g+204g}×$100%=15%;溶液具有均一性,将此溶液平均分成三等份,每一份的质量均为(36g+204g)÷3=80g,每一份溶液的溶质质量分数均为15%.
(1)取第一份,将温度升高到90℃,溶液的组成未发生改变,则此时溶质的质量分数为15%.
(2)设需要再溶解该物质的质量为x,(80g+x)×30%=80g×15%+x,x≈17.1g.
(3)设要加水的质量为y,根据溶液稀释前后溶质的质量不变,
则80g×15%=(80g+y)×7.5% y=80g.
故答案为:(1)15%;(2)17.1;(3)80.
点评 本题难度不大,掌握溶质的质量分数=$\frac{溶质质量}{溶液质量}×$100%、溶液具有均一性、溶液稀释前后溶质的质量不变是正确解答本题的关键.

练习册系列答案
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案
相关题目
16.下列有关微观粒子的说法中正确的是( )
| A. | 分子是由原子构成的 | |
| B. | 物质都是由离子构成的 | |
| C. | 原子中的粒子都不带电 | |
| D. | 分子是保持物质化学性质的唯一粒子 |
20.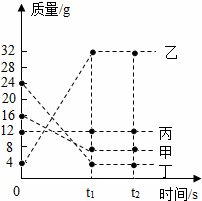 在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示,下列说法中不正确的是( )
在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示,下列说法中不正确的是( )
 在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示,下列说法中不正确的是( )
在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示,下列说法中不正确的是( )| A. | 该反应中,乙、丁的质量变化之比为7:5 | |
| B. | 该反应为化合反应 | |
| C. | 该反应中,甲、乙的质量变化之比为1:4 | |
| D. | 丙可能为该反应的催化剂 |
10.下列现象不能用质量守恒定律解释的是( )
| A. | 铁丝在氧气中燃烧后质量增大 | |
| B. | 20g食盐溶解到100g水中得到食盐水的质量为120g | |
| C. | 氯酸钾和二氧化锰混合加热后,试管中所剩物质的质量小于原混合物的质量 | |
| D. | 4g氢气和32g氧气恰好完全反应生成36g水 |
10.有化合价升降的反应是氧化还原反应,下列一定不是氧化还原反应的是( )
| A. | 2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C | B. | 2Na+2H2O═2NaOH+H2↑ | ||
| C. | Cl2+2NaI═2NaCl+I2 | D. | CO2+H2O═H2CO3 |
11.配置10%NaCl溶液的实验中,下列操作正确的是( )
| A. |  取用NaCl | B. |  称量NaCl | C. |  倾倒液体 | D. |  量取液体 |