题目内容
15.如图1是实验室制取气体的常用装置.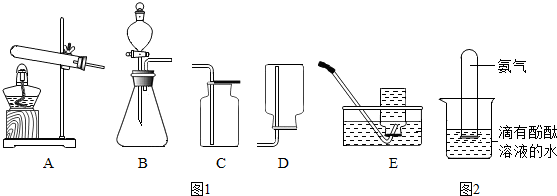
(1)写出一个用装置B制取气体的花学方程式:CaCO3+2HCl=CaCl2+H2O+CO2↑.
(2)实验室制取二氧化碳时,选用装置C收集气体,检验气体已收集满的方法是将一根燃烧的木条平放在集气瓶口,木条熄灭,证明满了.
(3)实验室选用装置A和D制取氨气(NH3),反应原理为:
Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑
①用收集到的氨气做如图2实验,观察到试管内液面上升几乎充满试管,溶液呈红色.由此得到的结论是氨气极易溶于水,水溶液呈碱性.
②收集氨气选用装置D而不是E的原因是氨气密度比空气小,极易溶于水.
分析 (1)装置B适用于固体与液体在常温下反应来制取气体;
(2)根据二氧化碳的性质来分析;
(3)据氨气的性质解答.
解答 解:(1)装置B适用于固体与液体在常温下制取气体,如用大理石或石灰石与稀盐酸反应来制取二氧化碳,或用二氧化锰作催化剂分解过氧化氢溶液制取氧气等;故填:CaCO3+2HCl=CaCl2+H2O+CO2↑(答案合理即可);
(2)二氧化碳的验满方法是:将一根燃烧的木条平放在集气瓶口,木条熄灭,证明满了.故答案为:将一根燃烧的木条平放在集气瓶口,木条熄灭,证明满了;
(3)①用收集到氨气做如图2实验,观察到试管内液面上升几乎充满试管,溶液呈红色,由此得到的结论是氨气极易溶于水,水溶液呈碱性;
②收集氨气选用向下排空气法而不能用排水法收集的原因是氨气密度比空气小,易溶于水.
故答案为:①氨气极易溶于水,水溶液呈碱性;②氨气密度比空气小,极易溶于水.
点评 通过回答本题知道了气体的制取方法及验满的方法,通过现象来推测物质性质的方法,并要灵活运用它们.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案
相关题目
4.将100g 98%的浓硫酸注入900g水中,所得稀硫酸中溶质的质量分数为( )
| A. | 9.8% | B. | 10.0% | C. | 10.9% | D. | 11.1% |
3.化学与生活密切相关,下列叙述中正确的是( )
| A. | 变霉的大米,要煮熟后食用 | |
| B. | 铵态氮肥与熟石灰混合使用会明显降低肥效 | |
| C. | 为了个人卫生,应提倡使用一次性的木筷和餐盒 | |
| D. | 人体缺锌会引起生长发育缓慢,因此青少年摄入锌元素越多越好 |
10.往某无色溶液中加稀盐酸,会产生一种可以使澄清石灰水变浑浊的气体,则原溶液中可能大量存在的离子是( )
| A. | Na+ | B. | Ca2+ | C. | Cu2+ | D. | H+ |
20.如图是四种微粒的结构示意图,下列有关各微粒的说法中,错误的是( )


| A. | ①容易得到电子 | B. | ①④的化学性质比较相似 | ||
| C. | ③是一种阴离子 | D. | ①②属于同种元素 |
7.如表是Ca(OH)2、NaOH的溶解度数据.请回答下列问题:
(1)要想把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,具体措施①加入氢氧化钙、②升高温度、③降低温度、④加入水、⑤蒸发水后再恢复到原温度、⑥加入生石灰.其中措施正确的是D(填字母).
A.②④⑤B.③④C.①⑤D.①②⑤⑥
(2)20℃时,欲测定NaOH溶液的pH,若先将pH试纸用蒸馏水润湿,再进行测定,则所测溶液的pH偏小(填“偏大”“偏小”或“不受影响”).
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | Ca(0H)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
| NaOH | 31 | 91 | 111 | 129 | 313 | 336 | |
A.②④⑤B.③④C.①⑤D.①②⑤⑥
(2)20℃时,欲测定NaOH溶液的pH,若先将pH试纸用蒸馏水润湿,再进行测定,则所测溶液的pH偏小(填“偏大”“偏小”或“不受影响”).
4.除去CaCl2溶液中含有少量HCl杂质时,可先向溶液中加入过量的某种物质,充分反应后再过滤,该物质是
( )
( )
| A. | CaO固体 | B. | CaCO3固体 | C. | Ca(OH)2固体 | D. | 铁粉 |
5.关于酒精(C2H5OH)的叙述错误的是( )
| A. | 酒精属于有机物 | B. | 酒精有5个氢原子 | ||
| C. | 酒精是可再生能源 | D. | 大量饮酒不利于身体健康 |