题目内容
9.多数食品易吸收空气中的水分变潮,并与空气中的O2 反应腐败.生产上多在食品上放入一包CaO粉未,使食品保持干燥.现已研究成功在食品中放入一包铁粉(包裹在多孔泡沫中)铁粉吸收水分和氧气变成铁锈,从而保护食品.下列说法不正确的( )| A. | 两干燥剂袋上都要有明显的“勿食”字样 | |
| B. | 生成铁锈的主要成分是氧化铁 | |
| C. | 铁粉干燥剂能与水和O2 发生化学反应 | |
| D. | CaO干燥剂保护食品的效果比铁粉干燥剂好 |
分析 根据铁生锈的条件、氧化钙的性质进行分析,氧化钙能与水反应生成氢氧化钙,可作干燥剂;铁生锈需要有氧气和水共同存在,在食品包装中加入铁粉不仅能吸水,还能除去氧气,据此进行分析判断.
解答 解:A、氧化钙具有腐蚀性,铁粉不能食用,两种干燥剂袋上都要有明显的“勿食”字样,故选项说法正确.
B、生成铁锈的主要成分是氧化铁,故选项说法正确.
C、铁粉干燥剂能与水和O2发生化学反应,故选项说法正确.
D、铁生锈需要有氧气和水共同存在,在食品包装中加入铁粉不仅能吸水,还能除去氧气,其干燥效果比氧化钙好,故选项说法错误.
故选:D.
点评 本题难度不大,掌握铁锈蚀的条件、氧化钙的化学性质并能灵活运用是正确解答本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19. 目前,一种人称“摇摇冰”的即冷即用饮料开始上市.所谓“摇摇冰”是指吸食前将饮料罐隔离层中的制冷物质和水混合摇动,能使罐中的饮料冷却.若该制冷物质可以在下列物质中选择,它应该是( )
目前,一种人称“摇摇冰”的即冷即用饮料开始上市.所谓“摇摇冰”是指吸食前将饮料罐隔离层中的制冷物质和水混合摇动,能使罐中的饮料冷却.若该制冷物质可以在下列物质中选择,它应该是( )
 目前,一种人称“摇摇冰”的即冷即用饮料开始上市.所谓“摇摇冰”是指吸食前将饮料罐隔离层中的制冷物质和水混合摇动,能使罐中的饮料冷却.若该制冷物质可以在下列物质中选择,它应该是( )
目前,一种人称“摇摇冰”的即冷即用饮料开始上市.所谓“摇摇冰”是指吸食前将饮料罐隔离层中的制冷物质和水混合摇动,能使罐中的饮料冷却.若该制冷物质可以在下列物质中选择,它应该是( )| A. | 食盐 | B. | 硝酸铵 | C. | 氢氧化钠 | D. | 酒精 |
20.某同学为探究镁、锌、铜、银的活动性顺序,设计如下实验流程,依据该流程设计,下面对物质①、②的选择合理的是( )
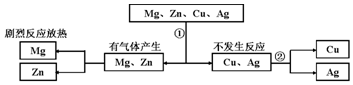

| A. | ①稀硫酸②硫酸汞 | B. | ①稀盐酸 ②硫酸锌 | ||
| C. | ①稀盐酸 ②硫酸亚铁 | D. | ①稀硫酸 ②氯化镁 |
4.已知:Si+2NaOH+H2O═Na2SiO3+2H2↑,2Al+2NaOH+2H2O═2NaAlO2+3H2↑,硅不能与盐酸反应,将含铁、铝、硅的合金样品分为等质量的两份,分别与足量的稀盐酸和烧碱溶液充分反应,测得放出氢气的质量相同.则该合金样品中铁、铝、硅的质量比不可能是( )
| A. | 112:81:28 | B. | 336:27:84 | C. | 324:135:36 | D. | 56:81:56 |
18.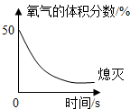 足量蜡烛(由碳、氢元素组成)在密闭集气瓶内(起始时常压)燃烧至熄灭,瓶内氧气体积分数随时间变化如图所示.下列说法正确的是( )
足量蜡烛(由碳、氢元素组成)在密闭集气瓶内(起始时常压)燃烧至熄灭,瓶内氧气体积分数随时间变化如图所示.下列说法正确的是( )
①起始阶段蜡烛燃烧比在空气中燃烧剧烈
②燃烧过程中,瓶内物质总质量不变
③蜡烛熄灭是由于瓶内氧气浓度过低
④若产物中二氧化碳与水分子个数相等,则反应后瓶内气体总质量增加.
 足量蜡烛(由碳、氢元素组成)在密闭集气瓶内(起始时常压)燃烧至熄灭,瓶内氧气体积分数随时间变化如图所示.下列说法正确的是( )
足量蜡烛(由碳、氢元素组成)在密闭集气瓶内(起始时常压)燃烧至熄灭,瓶内氧气体积分数随时间变化如图所示.下列说法正确的是( )①起始阶段蜡烛燃烧比在空气中燃烧剧烈
②燃烧过程中,瓶内物质总质量不变
③蜡烛熄灭是由于瓶内氧气浓度过低
④若产物中二氧化碳与水分子个数相等,则反应后瓶内气体总质量增加.
| A. | ③④ | B. | ①②③ | C. | ①②④ | D. | ①②③④ |
19.粗盐中含有泥沙等杂质,现将10g粗盐进行精制.
(1)为去除粗盐中的泥沙等不溶物质,需要进行溶解、过滤、蒸发等实验步骤才能完成.
(2)将40g水分成4等份依次加入到盛有10g粗盐的烧杯中,充分搅拌后,情况如下表:
由表中数据可得,10g粗盐含不溶性杂质2g.
(3)求最后所得溶液的溶质质量分数.
(1)为去除粗盐中的泥沙等不溶物质,需要进行溶解、过滤、蒸发等实验步骤才能完成.
(2)将40g水分成4等份依次加入到盛有10g粗盐的烧杯中,充分搅拌后,情况如下表:
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 加入的总水量/g | 10 | 20 | 30 | 40 |
| 剩余固体/g | 6.4 | 2.8 | 2 | 2 |
(3)求最后所得溶液的溶质质量分数.