题目内容
18.某兴趣小组为了探究铝、铁、铜三种金属的活动性,用铜丝、铁丝、铝丝和稀盐酸四种物质,设计了以下只用一只试管、取用一次盐酸的探究方案.请你和他们一起完善表的探究方案并回答有关问题.| 实验步骤 | 观察到的现象 | 化学方程式 |
| ①取适量盐酸于试管中,插入铁丝,充分作用. | 有气泡生成,溶液由无色 变成浅绿色. | Fe+2HCl═FeCl2+H2↑ |
| ②在①所得溶液中,插入 铜丝,充分作用. | 无明显现象 | |
| ③在②所得溶液中,插入 铝丝,充分作用. | 金属表面有一层黑色物质生成 | 2Al+3FeCl2=2AlCl3+3Fe |
分析 ①根据铁与盐酸的反应分析;
②根据现象为无明显现象,说明插入的金属不能与氯化亚铁反应;
③根据铝与氯化亚铁的反应分析.
解答 解:①由于铁与盐酸酸反应生成了氯化亚铁和氢气,所以观察到的现象是:在铁丝的表面有气泡产生,溶液由无色逐渐变为浅绿色;故填:浅绿;
②由现象为无明显现象,说明插入的金属不能与氯化亚铁反应.所以,在①所得的溶液中,插入的是铜丝;故填:铜丝;
③要比较铝、铁两种金属的活动性,在②所得的氯化亚铁溶液中插入铝丝,充分作用,现象是金属表面有一层黑色物质生成,故填:铝丝;2Al+3FeCl2=2AlCl3+3Fe.
结论:这三种金属的活动性顺序为:Al>Fe>Cu,故填:Al>Fe>Cu.
点评 在测定金属的活动性强弱时,根据与酸是否反应可以确定在金属活动顺序表中的大体位置,金属与可溶性盐的反应可以确定金属的活动性的强弱.

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目
6.钠原子失去1个电子后,发生变化的是( )
| A. | 电子层数 | B. | 质子数 | C. | 中子数 | D. | 相对原子质量 |
7.金刚石、石墨和C60的化学性质相似,物理性质却有很大差异.其原因是( )
| A. | 构成它们的原子大小不同 | B. | 构成它们的原子数目不同 | ||
| C. | 三者由不同原子构成 | D. | 它们碳原子的排列方式不同 |
6.下列实验操作错误的是( )
| A. |  闻气体的气味 | B. |  熄灭酒精灯 | ||
| C. |  量取液体 | D. |  连接玻璃管和胶皮管 |
13.下列反应属于置换反应的是( )
| A. | C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2 | B. | H2CO3═H2O+CO2↑ | ||
| C. | H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O | D. | C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O |
3.下列有关溶液的说法不正确的是( )
| A. | 物质的溶解度不一定都随温度升高而增大 | |
| B. | 溶剂不一定都是水,酒精、汽油等也可做溶剂 | |
| C. | 在鱼池中设立水泵,把水喷向空中可以增加水中氧气的溶解量 | |
| D. | 硝酸钾在20℃时溶解度是31.6g,则l00g 硝酸钾溶液中含有硝酸钾31.6g |
10.下列实验基本操作符合这一要求的是( )
| A. |  | B. |  | C. |  | D. |  |
8. 小红同学进行酸碱中和反应的实验(如图所示),她向氢氧化钠溶液中事先没有滴加指示剂.为了确定盐酸与氢氧化钠溶液中事先没有滴加指示剂,为了确定盐酸与氢氧化钠的反应程度,她从烧杯中取了少量溶液于试管中,并向试管中滴加几滴无色酚酞溶液,振荡,观察到试管中液体颜色没有变化,于是她对烧杯中的溶液进行了以下探究:
小红同学进行酸碱中和反应的实验(如图所示),她向氢氧化钠溶液中事先没有滴加指示剂.为了确定盐酸与氢氧化钠溶液中事先没有滴加指示剂,为了确定盐酸与氢氧化钠的反应程度,她从烧杯中取了少量溶液于试管中,并向试管中滴加几滴无色酚酞溶液,振荡,观察到试管中液体颜色没有变化,于是她对烧杯中的溶液进行了以下探究:
(1)写出盐酸与氢氧化钠溶液反应的化学方程式NaOH+HCl=NaCl+H2O,实验过程中,玻璃棒的作用是搅拌.
(2)小红认为此时烧杯中的溶液可能有以下三种情况:
①盐酸与氢氧化钠溶液恰好完全反应;②氢氧化钠有剩余;③盐酸过量;小明同学却判定不可能“氢氧化钠有剩余”,他的理由是观察到试管中溶液颜色没有变化,说明溶液一定不显碱性,所以不可能是氢氧化钠有剩余.
(3)他们共同设计了一个实验方案,欲对上述其他两种可能情况进行验证,请根据相关内容填写下表:
(4)经过讨论,他们认为利用下列几种物质代替锌粒,也可以达到验证目的,你认为其中不正确的是C(填序号).
A.生锈的铁钉B.碳酸钠粉末C.铜片D.铁片
(5)下列曲线能够表示小红所做实验中溶液pH变化趋势的是C(填序号).

(6)在实验室中,盐酸和氢氧化钠都要密封保存,盐酸需要密封保存的原因是盐酸具有挥发性,氢氧化钠需要密封保存的原因是(用化学方程式表示)2NaOH+CO2=Na2CO3+H2O.
 小红同学进行酸碱中和反应的实验(如图所示),她向氢氧化钠溶液中事先没有滴加指示剂.为了确定盐酸与氢氧化钠溶液中事先没有滴加指示剂,为了确定盐酸与氢氧化钠的反应程度,她从烧杯中取了少量溶液于试管中,并向试管中滴加几滴无色酚酞溶液,振荡,观察到试管中液体颜色没有变化,于是她对烧杯中的溶液进行了以下探究:
小红同学进行酸碱中和反应的实验(如图所示),她向氢氧化钠溶液中事先没有滴加指示剂.为了确定盐酸与氢氧化钠溶液中事先没有滴加指示剂,为了确定盐酸与氢氧化钠的反应程度,她从烧杯中取了少量溶液于试管中,并向试管中滴加几滴无色酚酞溶液,振荡,观察到试管中液体颜色没有变化,于是她对烧杯中的溶液进行了以下探究:(1)写出盐酸与氢氧化钠溶液反应的化学方程式NaOH+HCl=NaCl+H2O,实验过程中,玻璃棒的作用是搅拌.
(2)小红认为此时烧杯中的溶液可能有以下三种情况:
①盐酸与氢氧化钠溶液恰好完全反应;②氢氧化钠有剩余;③盐酸过量;小明同学却判定不可能“氢氧化钠有剩余”,他的理由是观察到试管中溶液颜色没有变化,说明溶液一定不显碱性,所以不可能是氢氧化钠有剩余.
(3)他们共同设计了一个实验方案,欲对上述其他两种可能情况进行验证,请根据相关内容填写下表:
| 实验方法 | 可能观察到的现象 | 结论 |
| 将少量锌粒放入试管中,然后从烧杯中取适量溶液至试管中 | 如果 有气泡产生 | 则盐酸过量,反应的化学方程式是: Zn+2HCl=ZnCl2+H2O |
| 如果 没有气泡产生 | 盐酸和氢氧化钠恰好完全反应 |
A.生锈的铁钉B.碳酸钠粉末C.铜片D.铁片
(5)下列曲线能够表示小红所做实验中溶液pH变化趋势的是C(填序号).

(6)在实验室中,盐酸和氢氧化钠都要密封保存,盐酸需要密封保存的原因是盐酸具有挥发性,氢氧化钠需要密封保存的原因是(用化学方程式表示)2NaOH+CO2=Na2CO3+H2O.
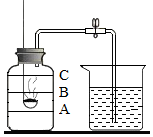 小华为了探究空气的成分,设计了如下实验(如图示):将导管上的弹簧夹夹紧,在燃烧匙中装满红磷,把燃烧匙放在酒精灯火焰上,点燃红磷后,迅速插入集气瓶内,塞紧橡皮塞.小华观察到红磷在瓶内继续燃烧,瓶内充满白烟.待集气瓶冷却到室温,瓶内白烟消失后,发现燃烧匙内红磷有剩余.把导管的另一端插入盛水的烧杯中,打开弹簧夹,水进入集气瓶.
小华为了探究空气的成分,设计了如下实验(如图示):将导管上的弹簧夹夹紧,在燃烧匙中装满红磷,把燃烧匙放在酒精灯火焰上,点燃红磷后,迅速插入集气瓶内,塞紧橡皮塞.小华观察到红磷在瓶内继续燃烧,瓶内充满白烟.待集气瓶冷却到室温,瓶内白烟消失后,发现燃烧匙内红磷有剩余.把导管的另一端插入盛水的烧杯中,打开弹簧夹,水进入集气瓶.