题目内容
9.下列关于“生活中的化学”的叙述中,不正确的是( )| A. | 胃酸过多可服用适量的小苏打 | |
| B. | 油锅着火可以立即用冷水浇灭 | |
| C. | 食用加碘食盐可预防甲状腺肿大 | |
| D. | 教室里能够闻到墙外的花香,是因为分子在不停的运动 |
分析 A、根据胃酸的主要成分是盐酸,盐酸能和小苏打反应进行解答;
B、根据油的密度比水小进行解答;
C、根据加碘食盐的碘元素可预防甲状腺肿大进行解答;
D、根据微粒的性质、特征进行分析进行解答.
解答 解:A、胃酸的主要成分是盐酸,盐酸能和小苏打反应,所以胃酸过多时,可服用适量的小苏打,故说法正确;
B、炒菜时油锅不慎着火,不能用冷水浇灭,因为油的密度比水小,油浮在水面上,起不到灭火的效果,应迅速盖上锅盖,可以起到隔离氧气的目的,从而灭火,故说法错误;
C、加碘食盐的碘元素可预防甲状腺肿大,故说法正确;
D、在花园里能闻到花香,是因为分子在不停的运动,通过运动花香的分子分散到周围的空气中,故说法正确.
故选:B.
点评 化学来源于生活,更服务于生活,与之相关考题会激发同学们的学习兴趣.

练习册系列答案
相关题目
20.某研究学习小组欲测定石灰石中碳酸钙的质量分数,采用的方法如下:取该石灰石样品20g,把80g稀盐酸分四次加入,实验过程所得数据如表格(已知石灰石样品中含有的二氧化硅等杂质不溶于水,不与稀盐酸反应).根据实验数据计算:
(1)表中n的数值为6.8.
(2)样品中碳酸钙的质量分数是66%.
(3)求盐酸中溶质的质量分数.
(1)表中n的数值为6.8.
(2)样品中碳酸钙的质量分数是66%.
(3)求盐酸中溶质的质量分数.
| 实验次数 | 加入稀盐酸的质量/g | 剩余固体的质量/g |
| 1 | 20 | 15 |
| 2 | 20 | 10 |
| 3 | 20 | 6.8 |
| 4 | 20 | n |
17.小强为自己准备的午餐食谱如图:
(1)妈妈建议增加凉拌黄瓜、清炒芹菜,是从营养均衡方面考虑黄瓜、芹菜可以为人体提供身体必须的维生素;
(2)联系课本知识,小强发现妈妈增加的芹菜富含铁元素,可有效预防贫血;
(3)从食谱中知道营养素主要有蛋白质、糖类、油脂、维生素、无机盐和水六大类.
| 主食 | 馒头、米饭 |
| 副食 | 红烧牛肉、清蒸鲈鱼 |
| 饮料 | 酸奶、白开水 |
(2)联系课本知识,小强发现妈妈增加的芹菜富含铁元素,可有效预防贫血;
(3)从食谱中知道营养素主要有蛋白质、糖类、油脂、维生素、无机盐和水六大类.
4.下列变化中,属于化学变化的是( )
| A. | 石蜡熔化 | B. | 纸张燃烧 | C. | 瓷碗破碎 | D. | 湿衣晒干 |
14.下列各组物质的溶液,不用其他试剂,只用观察和组内物质的溶液相互混合的方法,不能将它们一一鉴别出来的是( )
| A. | BaCl2 CuSO4 NaOH KNO3 | B. | Ba(NO3)2 Na2SO4 H2SO4 HCl | ||
| C. | KOH FeCl3 H2SO4 BaCl2 | D. | AgNO3 HCl K2CO3 CaCl2 |
1.2015年6月5日是第44个“世界环境日”,我国提出的主题是“践行绿色生活”.以下做法不符合该主题的是( )
| A. | 电视机长时间待机 | B. | 使用太阳能路灯照明 | ||
| C. | 绿化先行,富美漳州 | D. | 拆除九龙江两岸养殖场 |
13.形成温室效应的主要气体是( )
| A. | CO | B. | SO2 | C. | CO2 | D. | O3 |
14.复习课上,老师要求学生用不同的方法鉴别稀硫酸和氢氧化钠溶液,小东、小南两位同学取同一溶液分别进行如下实验:
【实验方案】
【提出问题】为什么我们取相同溶液而实验结论却不同呢?
【解决问题】小东、小南讨论后决定再用硫酸铜溶液进一步验证,结果观察到的现象是产生蓝色沉淀,于是一致认为该溶液是氢氧化钠溶液,为什么小南加入铝条会有气泡产生呢?通过查阅资料,他们发现初中常见金属中只有铝能与酸、碱反应,铝与氢氧化钠溶液反应的化学方程式是2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
【拓展延伸】利用老师要求鉴别的那两种溶液,测定镁铝铜合金中各成分的含量.实验设计如下:
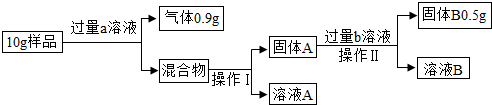
【回答问题】
(1)写出操作Ⅰ中玻璃棒的作用:引流.
(2)a溶液是氢氧化钠溶液,选择该溶液的理由是只能够把铝溶解.
(3)金属铜的质量为0.5g,固体A含有的物质是镁和铜,溶液A中所含溶质是NaOH、NaAlO2.
【实验方案】
| 实验步骤 | 实验现象 | 实验结论 | |
| 小东 | 用玻璃棒蘸取溶液滴到pH试纸上,对照比色卡并读出pH | pH试纸变色 pH>7(填“>”或“<”) | 该溶液是氢氧化钠溶液 |
| 小南 | 取适量溶液于试管中,加入经打磨过的铝条 | 有气泡产生 | 该溶液是稀硫酸 |
【解决问题】小东、小南讨论后决定再用硫酸铜溶液进一步验证,结果观察到的现象是产生蓝色沉淀,于是一致认为该溶液是氢氧化钠溶液,为什么小南加入铝条会有气泡产生呢?通过查阅资料,他们发现初中常见金属中只有铝能与酸、碱反应,铝与氢氧化钠溶液反应的化学方程式是2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
【拓展延伸】利用老师要求鉴别的那两种溶液,测定镁铝铜合金中各成分的含量.实验设计如下:

【回答问题】
(1)写出操作Ⅰ中玻璃棒的作用:引流.
(2)a溶液是氢氧化钠溶液,选择该溶液的理由是只能够把铝溶解.
(3)金属铜的质量为0.5g,固体A含有的物质是镁和铜,溶液A中所含溶质是NaOH、NaAlO2.
 图中A、B、C、D、E是初中化学常见的五种不同类别的物质. E是导致溫室效应的一种气体,图中“-”表示相连物质能发生化学反应,“→”表示两种物质间的转化关系(部分反应物、生成物及反应条件省略).
图中A、B、C、D、E是初中化学常见的五种不同类别的物质. E是导致溫室效应的一种气体,图中“-”表示相连物质能发生化学反应,“→”表示两种物质间的转化关系(部分反应物、生成物及反应条件省略).