题目内容
15.如图1是实验室制取CO2,并验证CO2性质的实验组合装置,根据装置解答下列问题: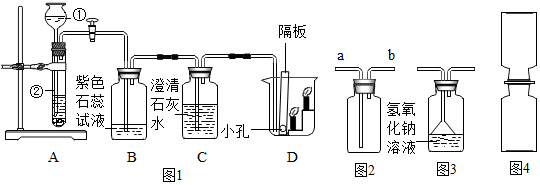
(1)写出标号仪器的名称:①分液漏斗 ②试管
(2)在装置B中可观察到的实验现象是:紫色逐渐变成红色,反应文字表达式为二氧化碳+水→碳酸
(3)装置C通常用于实验室检验CO2气体,其相关的反应文字表达式为:二氧化碳+氢氧化钙→碳酸钙+水.
(4)装置D中可观察到的现象是:底面蜡烛先熄灭,然后上面蜡烛再熄灭,
(5)实验室要制取NO2气体做微粒运动的演示实验.已知NO2可用铜片和浓硝酸溶液反应制取,同时生成硝酸铜和水.NO2是一种红棕色的气体,密度比空气密度大,易被氢氧化钠溶液吸收,能与水反应生成硝酸和NO.NO2和NO都有毒,易污染环境.
Ⅰ.实验室可用图1中的A装置制取NO2气体
Ⅱ.收集NO2可用如图3所示的装置,NO2应从a端(填“a”或“b”)通入.
Ⅲ.实验室通常在收集装置后还连接一套图3所示的装置,你认为这套装置的主要作用是:吸收二氧化氮,防止其污染空气.
Ⅳ.如图4所示,做微粒运动演示实验时,为缩短演示时间,NO2最好盛放在上(填“上”或“下”)面集气瓶中,另一瓶是空气,理由是:二氧化氮的密度比空气的密度大.如图4抽去玻璃片可看到:上瓶气体颜色逐渐变浅,下瓶气体颜色逐渐加深,最后颜色相同.
分析 (1)根据所学知识直接写出图中所标仪器的名称;
根据二氧化碳的如下性质回答2--4题:二氧化碳密度大于空气密度,不支持燃烧,易溶于水生成碳酸,可使紫色石蕊试液变红,二氧化碳遇石灰水变浑浊,常用此法检验二氧化碳;
(5)II、根据NO2密度比空气密度大分析;
Ⅲ、根据NO2是有毒气体,易被氢氧化钠溶液吸收分析;
Ⅳ、根据NO2的密度和从分子的性质进行分析.
解答 解:(1)图中①是分液漏斗,②是试管.故填:分液漏斗;试管;
(2)A中生成的二氧化碳溶于水生成碳酸,使B中的紫色石蕊试液变红,文字表达式是:二氧化碳+水→碳酸.
故填:紫色逐渐变成红色;二氧化碳+水→碳酸;
(3)二氧化碳使澄清石灰水变浑浊,常用于检验二氧化碳,文字表达式是:二氧化碳+氢氧化钙→碳酸钙+水;
故答案为:二氧化碳+氢氧化钙→碳酸钙+水;
(4)二氧化碳的密度大于空气的密度,并且不支持燃烧,所以D中的现象是:底面蜡烛先熄灭,然后上面蜡烛再熄灭;
故答案为:底面蜡烛先熄灭,然后上面蜡烛再熄灭;
(5))Ⅱ、因为NO2密度比空气密度大,用如图1所示的装置收集时,气体应从a端通入;
Ⅲ、因为NO2是有毒气体,易被氢氧化钠溶液吸收,所以图2所示的装置的主要作用是吸收二氧化氮,防止其污染空气.
Ⅳ、一切物质的分子都在不停的运动,将密度大的气体放在上面,密度小的气体放在下面会加快分子运动的速度.
故答案为:Ⅱ、a;
Ⅲ、吸收二氧化氮,防止其污染空气.
Ⅳ、上; 二氧化氮的密度比空气的密度大;上瓶气体颜色逐渐变浅,下瓶气体颜色逐渐加深,最后颜色相同.
点评 本题主要考查二氧化碳的物理、化学性质,以及根据所学知识和题干信息分析解题,需要同学们学好基础知识,以不变应万变.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.在学习化学的过程中,及时对所学知识进行整理,是一种好的学习方法.以下某同学归纳中,存在错误的是( )
| A. | 元素的化学性质与原子的最外层电子数有关 | |
| B. | 原子核都是由质子和中子构成 | |
| C. | 金刚石和石墨物理性质有很大差异原因在于碳原子的排列方式不同 | |
| D. | 一氧化碳和二氧化碳的化学性质差异在于分子的构成不同 |
10.如图是电解水的微观模型示意图,从中获得信息错误的是( )


| A. | 两种生成物的分子个数比为2:1 | |
| B. | 反应前后分子个数没有发生变化 | |
| C. | 反应前后原子的种类和数目没有变化 | |
| D. | 化学反应中,分子分为原子,原子不能再分 |
20.生理盐水是溶质质量分数约为0.9%的氯化钠溶液,现用1000克生理盐水给某病人输液,进入病人体内的氯化钠质量约为( )
| A. | 0.9克 | B. | 9克 | C. | 90克 | D. | 18克 |
7.化学与社会生活联系非常紧密,下列做法正确的是( )
| A. | 生活污水危害大,可任意排放 | |
| B. | 用甲醛浸泡海产品可以延长其保质期 | |
| C. | 禁止使用任何塑料制品可防止“白色污染” | |
| D. | 在酱油中加入铁强化剂,可预防缺铁性贫血 |
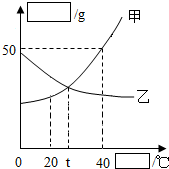 如图是甲、乙两种物质的溶解度曲线图:
如图是甲、乙两种物质的溶解度曲线图:
 家庭厨房就是一个化学小世界,“锅碗瓢盆”、“柴米油盐酱醋茶”中包含着许多化学知识.走进厨房,你会发现煤气罐被方便、价廉的管道天然气代替了,天然气代替煤气罐的优点是(1)环保、方便,便宜;天然气燃烧煮饭时的能量转化为(2)化学能转化为内能生活中自来水的净化经常用活性炭,活性炭在净化水的过程中的作用是(3)过滤不溶性杂质,吸附某些可溶性杂质,除去臭味.也用到漂白粉,漂白粉的制取是氯气和氢氧化钙溶液反应生成氯化钙和次氯酸钙(Ca(ClO)2)和一种常见的氧化物,写出制取漂白粉的化学方程式(4)2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,该反应前后氯元素的化合价变化为(5)0价变为-1价和+1价.
家庭厨房就是一个化学小世界,“锅碗瓢盆”、“柴米油盐酱醋茶”中包含着许多化学知识.走进厨房,你会发现煤气罐被方便、价廉的管道天然气代替了,天然气代替煤气罐的优点是(1)环保、方便,便宜;天然气燃烧煮饭时的能量转化为(2)化学能转化为内能生活中自来水的净化经常用活性炭,活性炭在净化水的过程中的作用是(3)过滤不溶性杂质,吸附某些可溶性杂质,除去臭味.也用到漂白粉,漂白粉的制取是氯气和氢氧化钙溶液反应生成氯化钙和次氯酸钙(Ca(ClO)2)和一种常见的氧化物,写出制取漂白粉的化学方程式(4)2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,该反应前后氯元素的化合价变化为(5)0价变为-1价和+1价.