题目内容
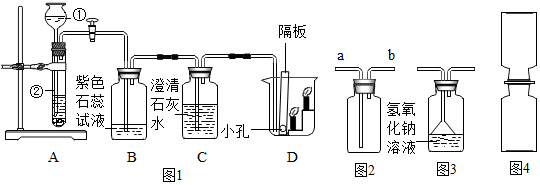
4.根据下列实验装置图,按要求回答下列问题:
(1)实验室用A装置制取氧气,反应的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
(2)实验室还可以用A装置制取二氧化碳气体,若要制取、收集一瓶干燥的二氧化碳气体,其装置接口的连接顺序是(用接口字母填空)a→f→e→c.
(3)验证二氧化碳已经集满的方法是:将燃着的木条平放于瓶口,若木条熄灭则已满.
(4)小明同学用F装置验证二氧化碳的性质,当通入二氧化碳一段时间后,试管①中溶液变红,产生该现象的原因是CO2+H2O=H2CO3(用化学方程式表示).G中观察到蜡烛由低到高依次熄灭,说明二氧化碳具有的性质是既不能燃烧,也不支持燃烧,密度比空气大.
分析 (1)根据装置的特点来确定制取氧气的原理;
(2)要制取和收集一瓶干燥的二氧化碳气体,要用E装置除去二氧化碳中的水分(浓硫酸具有吸水性),由于二氧化碳能溶于水且密度比空气大,所以只能用向上排空气法收集;
(3)据二氧化碳验满的方法解答;
(4)F装置中,试管①中产生的现象是紫色石蕊试液变红,因为二氧化碳和水反应生成碳酸,碳酸能使紫色石蕊试液;G中观察到蜡烛由低到高依次熄灭,说明二氧化碳具有的性质是:不燃烧也不支持燃烧,密度比空气大.
解答 解:(1)A装置适用于固液常温下制取气体,即是利用过氧化氢制取氧气,过氧化氢在二氧化锰的催化作用下分解的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
故填:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(2)制取二氧化碳选择A装置,干燥二氧化碳气体则通过浓硫酸,进气口是长管,这样气体能够与浓硫酸充分的接触而得到干燥,收集二氧化碳则采用向上排空气法,故连接的顺序为:a→f→e→c;故填:a→f→e→c;
(3)二氧化碳验满的方法是用燃着的木条放在瓶口,如果木条熄灭则说明瓶内已收集满二氧化碳;故填:将燃着的木条平放于瓶口,若木条熄灭则已满;
(4)F装置中,试管①中产生的现象是紫色石蕊试液变红,因为二氧化碳和水反应生成碳酸,碳酸能使紫色石蕊试液;G中观察到蜡烛由低到高依次熄灭,说明二氧化碳具有的性质是:不燃烧也不支持燃烧,密度比空气大;故填:CO2+H2O=H2CO3;既不能燃烧,也不支持燃烧,密度比空气大.
点评 本题考查了实验室制二氧化碳的原理以及气体制取、干燥和收集、验满,综合性比较强,关键是明确反应原理、洗气装置中导管长进短出等.

| A. | 碳酸钙溶于适量的稀盐酸 | |
| B. | 碳酸钙溶于适量的水中 | |
| C. | 锌与过量的稀硫酸混合 | |
| D. | NaOH溶液与CuSO4溶液按适当比例混合使其恰好反应 |
| 浓硫酸(H2SO44500毫升 | |
| 溶质的质量分数 | 98% |
| 密度 | 1.84克/厘米3 |
| 相对分子质量 | 98 |
| 强腐蚀性,阴冷,密封储藏 | |
(2)若将这100毫升浓硫酸与500克水均匀混合,所得稀硫酸的质量分数是多少?(保留2位小数)
(3)他将一个密度为1.14×103kg/m3,体积为20cm3耐酸小球放在稀硫酸中静止时受到的浮力.(g取10牛/千克)
 如图是“电解水实验”的装置图,根据所学知识回答问题:
如图是“电解水实验”的装置图,根据所学知识回答问题: