题目内容
5.某化学兴趣小组想研究影响过氧化氢(H2O2)分解速度的因素.取四支试管,在2、3、4号试管中分别加入0.2克二氧化锰 (MnO2)粉末,然后在四支试管中分别加入等量的过氧化氢溶液(溶质质量分数如下表所示),观察气泡产生的速度,记录如下:| 试管编号 | 1 | 2 | 3 | 4 |
| H2O2溶液的溶质质量分数 | 5% | 5% | 10% | 15% |
| MnO2质量 | 0克 | 0.2克 | 0.2克 | 0.2克 |
| 气泡产生的速度 | + | +++ | ++++ | +++++ |
(2)为了检验产生的气体是否为氧气,请你写出检验的操作方法:将带火星的木条伸入试管中,如果木条复燃,则证明该气体为氧气.
(3)小米同学提出,通过上述实验不能证明MnO2是该反应的催化剂.于是,化学兴趣小组展开了讨论,最后一致认为:还需证明二氧化锰在化学反应前后质量和化学性质不变.他们继续进行了实验.
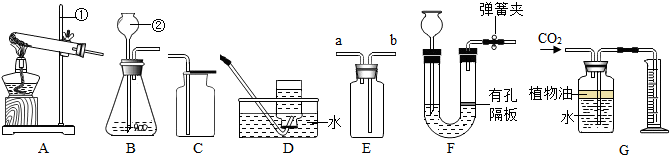
(4)可利用过滤法回收剩余溶液中的二氧化锰粉末.在过滤过程中,如图仪器不需要的有BC(填序号).

过滤后,他们发现滤液仍然浑浊,其可能原因是滤纸破损.(任写一点)
分析 (1)根据实验中所给数据考虑解答;
(2)根据氧气的助燃性进行解答;
(3)根据二氧化锰在该实验中起催化作用进行解答;
(4)根据过滤中用到的仪器进行解答;
(5)根据过滤过程中的注意事项进行解答.
解答 解:(1)由题目中的数据可知,在二氧化锰的量一定的情况下,双氧水溶液的溶质质量分数越大,气泡产生的速度越快,所以该实验研究的问题是过氧化氢分解的速度与双氧水溶液的浓度的关系;
(2)因为氧气具有助燃性,用带火星的木条检验产生的气体是否为氧气.检验的方法:将带火星的木条伸入试管中,如果木条复燃,则证明该气体为氧气.
(3)二氧化锰在该实验中加快了过氧化氢反应放出氧气的速率,但本身的质量和化学性质不变,二氧化锰在此实验中的作用是催化作用;
(4)过滤中用到的仪器:玻璃棒、烧杯、漏斗、铁架台等;而不需要天平和酒精灯;若经过过滤操作后,所得的液体仍呈现浑浊,其原因可能是漏斗内的滤纸有破损缘和漏斗内液面高于滤纸的边缘或滤纸破损或盛滤液的烧杯不干净;
故答案为:(1)过氧化氢溶液的溶质质量分数;MnO2(或者催化剂)
(2)将带火星的木条伸入集气瓶内;
(3)质量;化学性质;
(4)B;滤纸破损(答案合理即可).
点评 通过回答本题知道了影响过氧化氢反应速度的因素、氧气的助燃性以及过滤中的注意事项.操作对比实验,在分析实验数据的基础上得到正确结论,是对学生分析能力的考查.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
15.“绿色化学”是21世纪化学发展的主导方向,“绿色化学”要求从根本上消除污染,它包括“原料的绿色化”、“化学反应绿色化”、“产物绿色化”等内容.其中(化学反应绿色化)要求原料物质中所有的原子完全被利用且全部转化入期望的产品中.下列反应中符合“化学反应绿色化”的是( )
| A. | 用氯酸钾和二氧化锰制取氧气 | B. | 工业上制取氧气 | ||
| C. | 2C2H4+O2→2C2H40 | D. | 天然气燃烧生成二氧化碳和水 |
13.下列物质的用途中,利用了其物理性质的是( )
| A. | 稀有气体通电时会发出五颜六色的光 | |
| B. | 氧气用于炼钢 | |
| C. | 氮气充入食品包装袋防腐 | |
| D. | 氢气可作高能燃料 |
10.区别氢气、空气、氧气和氮气四种气体,最简单的方法是( )
| A. | 测量四种气体的密度 | B. | 闻气体的气味 | ||
| C. | 用燃着的小木条 | D. | 观察气体的颜色 |
17. 元素周期表是化学学习和研究的重要工具之一.下图是元素周期表的一部分.
元素周期表是化学学习和研究的重要工具之一.下图是元素周期表的一部分.
(1)表中不同种元素最本质的区别是A(填序号).
A.质子数不同 B.最外层电子数不同 C.电子数不同 D.中子数不同
(2)硅元素的相对原子质量为28(取整数),它属于非金属(填“金属”或“非金属”)元素
(3)氧元素位于第三周期,其核电荷数为8,氧原子最外层电子数为6,在化学反应中易得到(填“得到”或“失去”)电子,表中与其化学性质相似的元素是硫.
(4)如图所示为某粒子结构示意图,若为原子,则X-Y等于10,若X-Y等于9,则该粒子的符号是Cl-.
 元素周期表是化学学习和研究的重要工具之一.下图是元素周期表的一部分.
元素周期表是化学学习和研究的重要工具之一.下图是元素周期表的一部分.| 族 周期 | IA | 0 | ||||||
| 1 | 1 H 1.008 | ⅡA | ⅢA | ⅣA | V A | ⅥA | ⅦA | 2 He 4.003 |
| 2 | 3 Li 6.941 | 4 Be 9.012 | 5 B 10.8l | 6 C 12.01 | 7 N 14.0l | 8 O 16.00 | 9 F 19.00 | 10 Ne 20.18 |
| 3 | 11 Na 22.99 | 12 Mg 24.31 | 13 Al 26.98 | 14 Si 28.09 | 15 P 30.97 | 16 S 32.06 | 17 Cl 35.45 | 18 Ar 39.95 |
A.质子数不同 B.最外层电子数不同 C.电子数不同 D.中子数不同
(2)硅元素的相对原子质量为28(取整数),它属于非金属(填“金属”或“非金属”)元素
(3)氧元素位于第三周期,其核电荷数为8,氧原子最外层电子数为6,在化学反应中易得到(填“得到”或“失去”)电子,表中与其化学性质相似的元素是硫.
(4)如图所示为某粒子结构示意图,若为原子,则X-Y等于10,若X-Y等于9,则该粒子的符号是Cl-.


 化学用语可准确、简洁地记录、表达和交流化学信息.请用化学符号填空:
化学用语可准确、简洁地记录、表达和交流化学信息.请用化学符号填空: