��Ŀ����
2�� ���ϣ�����Ҫ�������ס�������벻����ˮ���������������ϼ�û��ˮ��û�п�������ѧ�ҷ��������ɳ���к��зḻ�ĺ��������ɷ�ΪTiO2��Fe2O3�Ļ���������Щ��ʯ����CO����ԭ�������������Ѻ���������������ԭ�����Եõ���ˮ��������Щ��ʯͨ�磬�����Դ��з����������
���ϣ�����Ҫ�������ס�������벻����ˮ���������������ϼ�û��ˮ��û�п�������ѧ�ҷ��������ɳ���к��зḻ�ĺ��������ɷ�ΪTiO2��Fe2O3�Ļ���������Щ��ʯ����CO����ԭ�������������Ѻ���������������ԭ�����Եõ���ˮ��������Щ��ʯͨ�磬�����Դ��з������������1�����������д�����Ȼ�������������ȶ��ֽ����������������������Au��������Ͻ����л���ijЩ����������Ͻ������������������г�ַ�Ӧ��Ȼ����ˣ�ʣ��Ĺ����п��Ի��յõ��Ľ��������C
A��Fe B��Au��Fe C��Ag��Au D��Fe��Ag
��2���ݿ�ѧ��Ԥ�⣬����������������Ű���ֵĺ���He-3������ԭ�Ӻ���������Ϊ2��������Ϊ1��ÿ�ٶֺ���He-3���˾۱����ͷŵ������൱��Ŀǰ����һ�����ĵ����������й��ں���He-3��Ԫ�ص�˵����ȷ����D
A��ԭ�Ӻ��������Ϊ3
B�����ԭ������Ϊ2
C��ԭ�ӽṹʾ��ͼΪ

D��ԭ�ӽṹʾ��ͼΪ
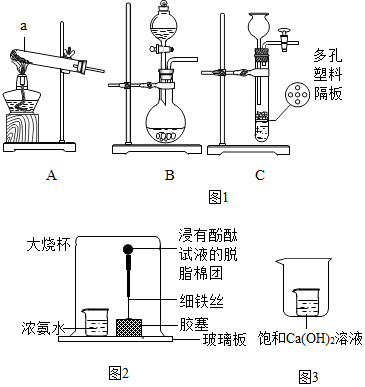
��3�����϶�һ�š�����Ļ���ƽ�����װ��Һ̬�£���A��ʾ���������⣨H2O2�������ǻ��ʱ�ķ�Ӧ����ʽΪ��2H2O2+A�TN2+4H2O�����£�A���Ļ�ѧʽΪD
A��N2H2 B��N2H4O2 C��NH2D��N2H4
��4��������CO����ԭTiO2��Fe2O3�Ļ�������������Ѻ�����װ����ͼ��ʾ���Իش�
��д��A�з�����Ӧ��ѧ����ʽ������һ����2CO+TiO2$\frac{\underline{\;����\;}}{\;}$Ti+2CO2����3CO+Fe2O3 $\frac{\underline{\;����\;}}{\;}$3CO2+2Fe����
����CO��ԭ�����������Ѻ����Ļ�������ʲô�������������������ʷֿ��ô���������
�۾Ͳ���˳��������λͬѧ�����˷��磮С����Ϊ�ȵ�ȼC��A�еľƾ��ƣ�Ȼ����ͨCO��С��������ԣ�����������CO�벣�����ڿ�����ϼ��ȿ��ܱ�ը��
��5����ѧϰ�˽��������ʺ�ѧʵ��С��ͬѧ�ԡ�21���͵���Ҫ���������Ѻ��ѺϽ𡱲�������Ȥ�����ǽ���������̽����������һͬ���룮
�������ϣ�
A���ѵ�Ӳ���������࣬����������ֻ��ͬ���������һ�룬�ѵ��ܶ���Ȼ�����Դ�һ�㣬������Ӳ��ȴ������������
B�������ڻ�ѧ���ʱȽϻ��õĽ��������ڳ������ѵĿ���ʴ�Ժ�ǿ����ʹ���ѷ��ں�ˮ�����꣬ȡ�����Թ��������
C���ѺϽ���������кܺõġ������ԡ������������ֿܵ�������ĸ�ʴ������
���̽����
���������Ľ��������һ��ǿ��
��������衿���ѵĽ�����Ա���ǿ��
�����ʵ�顿�����ѷ�������������Һ�й۲죮
���ѵĻ�Ա���ǿ������ʵ����ֵ������ǣ��ѱ������ɺ�ɫ���ʣ���Һ��dz��ɫ��Ϊ��ɫ��
�����DZȽϻ��õĽ�����Ϊʲô��ʴ��ȴ��ǿ�����ܵ�ԭ���ǣ����������������������Ӧ����һ�����ܵ�����Ĥ��
����Ҫ�Ƚ���Ƭ����Ƭ��Ӳ�ȣ���ķ����ǣ���̻���
˼����Ӧ�ã�
�����ʵ�������һ���̶��Ͼ�����������;�������������C�ж��ѵ���;��������ǣ�
��6����ұ��2310t������3%����������Ҫ��Fe2O376%����������������������Ƕ��٣�����д��������̣�����һλС����
���� ��1�����ݽ������˳�����Ӧ�÷������ڽ������˳����У�λ����ǰ��Ľ��������ᷴӦ��
��2������ԭ�ӵ����֪ʶ���н�����Ŀ����ҪҪ�õ���֪ʶ�㣺��ԭ�ӽṹʾ��ͼ�DZ�ʾԭ�Ӻ˵�����͵��Ӳ��Ų���ͼʾ��ʽ��ԭ�ӽṹʾ��ͼ�ֲ��Ų����ɣ���һ�����2�����ӣ��ڶ������8�����Ӣ���ԭ���У�����������=��������������ԭ��������������+���������ݴ˷������ɣ�
��3�����������غ㶨�ɿ����ж����ʵĻ�ѧʽ��
��4���ٸ���һ����̼��ԭTiO2��Fe2O3�ķ�Ӧд����Ӧ�ķ���ʽ��
�ڸ������ܱ��������������ش�
�۸���һ����̼�ж�����Ⱦ����������
��5���ٱȽ����ֽ����Ļ�ԣ����Լ���һ�ֱ���һ�ֻ��ǿ��
�ڸ����ѵ����ʷ������ǣ�
�۸����ṩ����Ϣ�����ԱȽ��Ѻ����Ļ�ԣ�Ȼ����������ƶ���;��
��6�����ݲ������ʵĻ�ѧ����ʽ�йؼ���������
��� �⣺��1���ɽ������˳���֪����Ŀ�����������Ļ��Ϊ��Fe����H����Ag��Au��������Ͻ������������������г�ַ�Ӧ��Ȼ����ˣ�ʣ��Ĺ����п��Ի��յõ��Ľ��������Ag��Au��
��2��A����ΪHe-3ԭ�Ӻ��ں���2�����ӣ���������λ����ɣ��ɺ��������=�����������ɵã����������ӦΪ2����A����
B����Ϊ�����ԭ��������������+������=1+2=3����B����
C������������Ϊ2��HeԪ�ص�ԭ�ӽṹʾ��ͼԲȦ������������ֵӦΪ2����C����
D��ԭ�ӽṹΪ����2�����ӣ�����2�����ӣ��ýṹʾ��ͼ���ϸ��ص��Һ�������Ų���ȷ����D��ȷ��
��ѡD��
��3���ɷ�Ӧ2H2O2+A�TN2+4H2O��֪����Ӧ������ԭ�ӣ�8������ԭ�ӣ�4������ԭ�ӣ�2�����������غ㶨�ɷ�Ӧǰ��ԭ�ӵ����༰��Ŀ���Ƴ���A������ԭ�Ӹ���Ϊ��8-4=4������ԭ�Ӹ���Ϊ��2-0=2������A�Ļ�ѧʽӦΪ��N2H4��
��4�����ڼ��ȵ������£�һ����̼�ܽ��������ѡ���������ԭΪ�ѡ�������Ӧ�ķ���ʽ�ǣ�2CO+TiO2$\frac{\underline{\;����\;}}{\;}$Ti+2CO23CO+Fe2O3 $\frac{\underline{\;����\;}}{\;}$3CO2+2Fe��
���������ܱ��������������Կ��ô������������ɵ��Ѻ����ֿ���
����һ����̼��ԭ������ʱ��С����Ϊ��ͨһ��ʱ��CO�ſգ�Ȼ���ٵ�ȼC��A�еľƾ��ƣ�С����Ϊ���������ã����������ǣ�����CO��ɢ����������ɿ�����Ⱦ��
��5���ٱȽ��������Ľ��������һ��ǿ�����Լ����ѱ���ǿ����������ǰ��Ľ����ܰѺ���Ľ�����������Һ���û��������ʵ�飬���ƲⷴӦ�������ԣ�
��������衿���ѵĽ�����Ա���ǿ��
�����ʵ�顿�����ѷ�������������Һ�й۲죮
���ѵĻ�Ա���ǿ������ʵ����ֵ������ǣ��ѱ������ɺ�ɫ���ʣ���Һ��dz��ɫ��Ϊ��ɫ��
�����DZȽϻ��õĽ�������ʴ��ȴ��ǿ��ԭ��������ѵı������γ����ܵ������ﱣ��Ĥ��
����Ҫ�Ƚ���Ƭ����Ƭ��Ӳ�ȣ������ǣ���̣�
�����ʵ�������һ���̶��Ͼ�����������;�����Ѿ��С�������ԣ����������ֿܵ�������ĸ�ʴ����������������ǣ� �ܶ�С��Ӳ�ȴ������ڷɻ����ɴ��Ⱥ��չ��ߣ�
��6�����躬������76%���������������������Ϊx
3CO+Fe2O3$\frac{\underline{\;����\;}}{\;}$2Fe+3CO2
160 112
76%x 2310t��1-3%��
$\frac{160}{112}=\frac{76%x}{2310t��1-3%��}$ ��ã�x��4211.8t
�ʴ�Ϊ����1��C�� ��2��D�� ��3��D����
��4����2CO+TiO2$\frac{\underline{\;����\;}}{\;}$Ti+2CO2����3CO+Fe2O3 $\frac{\underline{\;����\;}}{\;}$3CO2+2Fe��������������
��CO�벣�����ڿ�����ϼ��ȿ��ܱ�ը
��5���١�������衿���ѵĽ�����Ա���ǿ��
�����ʵ�顿�����ѷ�������������Һ�й۲죮
�����ǣ��ѱ������ɺ�ɫ���ʣ���Һ��dz��ɫ��Ϊ��ɫ��
�ڳ��������������������Ӧ����һ�����ܵ�����Ĥ��
�۷����ǣ���̻�����;�� ������ǣ�
��6����Ҫ��������76%����������������4211.8��
���� ������һ�����֪ʶ�����⣬����Ĺؼ��������йؽ����Ļ��˳���Ӧ���Լ�����ұ�����й�֪ʶ��

 �̲�ȫ���ִʾ�ƪϵ�д�
�̲�ȫ���ִʾ�ƪϵ�д� ��ʵ�����У���ѧ��ȤС���ͬѧ������һƿ���ڷ��õ�Ca��OH��2��ĩ״�Լ������ǶԸ��Լ������˶���ʵ���������ȡ�Լ�19.8g������ƿ�У�����30.2g��ˮ�������������ƿ�����εμ�25g�����ַ�Ӧ����ò���������ͼ�����£�������й���Ϣ�ش����⣮
��ʵ�����У���ѧ��ȤС���ͬѧ������һƿ���ڷ��õ�Ca��OH��2��ĩ״�Լ������ǶԸ��Լ������˶���ʵ���������ȡ�Լ�19.8g������ƿ�У�����30.2g��ˮ�������������ƿ�����εμ�25g�����ַ�Ӧ����ò���������ͼ�����£�������й���Ϣ�ش����⣮| ��1�� | ��2�� | ��3�� | ��4�� | ��5�� | ��6�� | |
| ���������������g�� | 25 | 25 | 25 | 25 | 25 | 25 |
| ��ƿ�����ʵ�������g�� | 75 | 100 | a | 150 | 172.8 | 197.8 |
��2��b����ֵΪ2.2��
��3��������Լ����������Ƶ��������������������������д��������̣��������һλС������
���������ϡ���ɫ����ˮ����ͭ��ˮ������ɫ��
��ʵ����ơ�
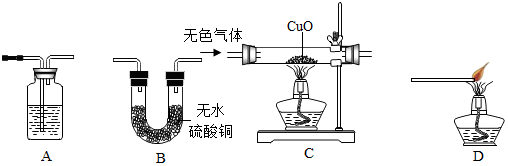
����ͼװ��A��ʢ�ŵ�Һ��������ʯ��ˮ��
����ͼװ�õ���ȷ����˳���ǣ�CBAD������ĸ����ÿ��װ������һ�Σ���
�����в��롿��װ��������ȷ���й���ɫ����ɷֵIJ���Ͷ�Ӧ��ʵ���������±���
| ��ɫ����ijɷ� | ��Ӧ��ʵ������ | ||
| װ��A�е�Һ�� | װ��B�еĹ��� | װ��C�еĹ��� | |
| ����һ��ֻ��CO | ����� | ���������� | ��� |
| ���������һ����̼������ | ����� | ���� | |
| ��������ֻ��H2 | �ޱ仯 | ���� | |
����չ���졿��Ԫ�ؿ����γ�����������ֱ���Fe2O3��Fe3O4 ��FeO����ɫ������CuO��Ϊij��ɫ��ĩ��������һ�ֻ���������������ɣ���������ͼװ�ð�ԭ����˳�����ʵ�飬��ַ�Ӧ������������ȫ��ת��Ϊ����װ��C������һ���Ľ��ǽ��ƾ��ƻ��ɾƾ���ƣ�
�����ݷ�������������ʵ����ÿһ�����ն�����ȫ�ģ�����ɫ��ĩ������Ϊ4.8g����Ӧ��װ��A������Ϊ1.1g��װ��B������Ϊ0.9g�����ɫ��ĩ�ijɷ������������������������Ļ���
 ��������ʵ�鳣��װ�ã��ش��й����⣮
��������ʵ�鳣��װ�ã��ش��й����⣮