题目内容
15.某化学课堂围绕“酸碱中和反应”开展探究活动:将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中.(1)该反应的化学方程式H2SO4+2NaOH=Na2SO4+2H2O;
【提出问题】实验中未观察到明显现象,疑问:反应后溶液中溶质是什么?
【假设猜想】猜想一:只有Na2SO4
猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4、H2SO4和NaOH
猜想四:有Na2SO4和NaOH;
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的猜想是三,理由是H2SO4和NaOH在溶液中不能共存.
【查阅资料】①Na2SO4溶液显中性.
②Al与强碱NaOH溶液反应生成偏铝酸钠(NaAlO2)和氢气.
【实验探究】(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有NaOH
(2)为了验证其余猜想,进行如下探究
| 方案 | 1 | 2 | 3 | 4 |
| 实验操作 | 取中和反应后的溶液少许于试管中 | |||
| 放入打磨后的铝片 | 滴加Na2CO3溶液 | 滴加BaCl2溶液 | 滴加无色酚酞 试液 | |
| 实验现象 | 铝片逐渐溶解,产生大量气泡 | 产生大量气泡 | 产生白色沉淀 | 溶液变 红色 |
| 结论 | 猜想二成立 | |||
【知识拓展】生活中能否用铝制品来盛放强碱性溶液?不能(填“能”或“不能”)
分析 【学生板演】硫酸和氢氧化钠反应生成硫酸钠和水,注意化学式的写法和配平;
【假设猜想】根据酸碱不能共存判断不合理的猜想;
【实验探究】根据碳酸钠和硫酸反应能生成二氧化碳气体,硫酸钠能与氯化钡反应生成白色沉淀,酸性溶液能使无色酚酞溶液变红解答;
检验一种物质时要排除其他物质的干扰,硫酸钠也能与氯化钡反应生成白色沉淀.
【知识拓展】铝能和氢氧化钠反应生成偏铝酸钠和氢气,
解答 解:【学生板演】硫酸和氢氧化钠反应生成硫酸钠和水,化学方程式为H2SO4+2NaOH═Na2SO4 +2H2O;
【假设猜想】硫酸和氢氧化钠反应生成硫酸钠和水,酸或碱可能过量,也可能恰好反应,恰好反应后溶液中的溶质为硫酸钠,故猜想一为氢氧化钠和硫酸钠及硫酸,酸碱不能同时过量,因为酸碱不能共存,会继续反应,故猜想一不合理;
【实验探究】(1)硫酸铜和氢氧化钠反应能生成氢氧化铜蓝色沉淀,因此溶液中滴加几滴CuSO4溶液,无明显变化,说明溶液中一定没有氢氧化钠.
(2)溶液中有硫酸,滴加碳酸钠后,碳酸钠会和硫酸反应生成二氧化碳气体,因此会看到产生气泡.硫酸钠能与氯化钡反应生成白色沉淀,酸性溶液能使无色酚酞溶液变红;
硫酸钠能与氯化钡反应生成白色沉淀,反应的化学方程式为:Na2SO4+BaCl2=2NaCl+BaSO4↓;
检验一种物质时要排除其他物质的干扰,硫酸钠也能与氯化钡反应生成白色沉淀,故不能证明溶液中一定存在硫酸;
【知识拓展】因为铝能与碱性物质反应,故生活中不能用铝制品来盛放强碱性溶液,故填:不能;
(2)故答案为:【学生板演】H2SO4+2NaOH=Na2SO4+2H2O;
【假设猜想】有Na2SO4和NaOH;猜想三;H2SO4和NaOH在溶液中不能共存;
【实验探究】(1)NaOH;
(2)
| 方案 | 1 | 2 | 3 | 4 |
| 实验操作 | 取中和反应后的溶液少许于试管中 | |||
| 放入打磨后的铝片 | 滴加Na2CO3溶液 | 滴加BaCl2溶液 | 滴加 无色酚酞 试液 | |
| 实验现象 | 铝片逐渐溶解,产生大量气泡 | 产生 大量气泡 | 产生 白色沉淀 | 溶液变 红色 |
| 结论 | 猜想二成立 | |||
【知识拓展】不能.
点评 此题通过中和反应考查了化学方程式的书写,实验方案设计、实验操作以及实验方案的评价,解答时要全面审题,认真解答.

 名校课堂系列答案
名校课堂系列答案| A. | 使用可降解塑料代替传统塑料,有利于减轻“白色污染” | |
| B. | 稀土是储量较少、不可再生的金属资源 | |
| C. | 一种元素在同一化合物可以显示不同的化合价 | |
| D. | 催化剂能改变化学反应的速率,而本身的质量和性质在化学反应前后都不会改变 |
【提出问题】久置固体的成分是什么?
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3.
【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁.
【实验探究】甲同学的方案:
| 实验操作 | 实验现象 | 实验结论 |
取少量固体于试管中,滴 加足量的稀盐酸(或稀硫酸). | 固体逐渐消失,有大量无色气体产生,得到浅绿色溶液. | 固体中一定含有Fe(或铁粉), 一定不含Fe2O3. |
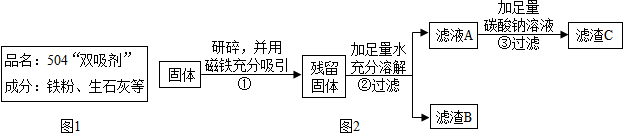
他设计如图2实验方案继续验证.
(1)步骤①样品用磁铁吸引前需经过研碎,其中研碎的目的是增大接触面积,使得铁粉能够充分吸引;
(2)②中固体溶解时放出大量热,由此可以判断固体中一定含有CaO(或氧化钙).
(3)③中反应的化学方程式是Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
乙同学对滤渣B又进行探究.
| 实验操作 | 实验现象 | 实验结论 |
| 取少量固体于试管中,滴加足量的稀盐酸,并将气体通入澄清石灰水 | 固体逐渐消失、有气泡产生、 澄清石灰水变浑浊、溶液呈黄色. | 固体中一定含有CaCO3和Fe2O3. |
| 实验内容 | 实验结论 | |
| A | 带有火星的木条置于氧气瓶中,木条复燃 | 氧气有可燃性 |
| B | CO2通入紫色石蕊试液中,石蕊试液变红色 | CO2具有酸性 |
| C | 稀盐酸滴入氢氧化钠溶液中,未观察到明显现象 | 没有发生化学反应 |
| D | 氯化钙溶液滴入某溶液中,出现白色沉淀 | 溶液中可能含有CO32- |
| A. | A | B. | B | C. | C | D. | D |
实验一:取5mL氢氧化钠溶液于烧杯中,滴入几滴酚酞溶液,可观察到现象为溶液变红,然后加入稀盐酸,用玻璃棒搅拌,溶液褪为无色,有关的反应方程为HCl+NaOH═NaCl+H2O;
实验二:对实验一反应后溶液中的溶质进行探究.
【提出猜想】
猜想一:只有NaCl 猜想二:有NaCl和NaOH猜想三:有NaCl和HCl
你认为猜想二不合理.
【设计实验】
| 实验操作 | 实验现象 | 实验结论 |
| 取反应后的溶液于试管中,加入石蕊试液 | 溶液变红 | 猜想三成立 |
| A. | 石蜡熔化 | B. | 纸张燃烧 | C. | 粮食霉变 | D. | 烟花爆炸 |

| A. | 都可采取升温的方法 | B. | 都可采取降温的方法 | ||
| C. | 都可采取加原溶质的方法 | D. | 都可采取加水的方法 |
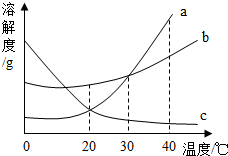 如图所示是甲、乙、丙三种物质的溶解度曲线,在20℃时,分别取等质量的三种物质的饱和溶液放入三只烧杯中,然后向溶液分别加入等质量的相应固体物质,再将温度升高到40℃,结果甲物质全部溶解,丙物质部分溶解,试回答下列问题:
如图所示是甲、乙、丙三种物质的溶解度曲线,在20℃时,分别取等质量的三种物质的饱和溶液放入三只烧杯中,然后向溶液分别加入等质量的相应固体物质,再将温度升高到40℃,结果甲物质全部溶解,丙物质部分溶解,试回答下列问题: