题目内容
15.下列实验方案中,合理的是( )| A. | 要检验混合气体中含有CO和CO2:先将气体通过灼热氧化铜,再通过澄清石灰水 | |
| B. | 除去Ba(NO3)2溶液中的HNO3:加入过量的BaCO3固体,过滤 | |
| C. | 除去CO2中的HCl气体和H2O:将混合气体依次通过足量NaOH溶液和浓H2SO4 | |
| D. | 验证氢氧化钠和盐酸反应:先向氢氧化钠溶液中加少量稀盐酸,再放少量氧化铜 |
分析 A、根据检验二氧化碳使用澄清的石灰水,检验一氧化碳可铜灼热的氧化铜,一氧化碳与氧化铜反应生成铜和二氧化碳,进行分析判断.
B、除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
C、除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
D、根据氢氧化钠溶液与稀盐酸反应生成氯化钠和水,氧化铜能与稀盐酸反应生成氯化铜和水,进行分析判断.
解答 解:A、要检验混合气体中含有CO和CO2,先将气体通过澄清石灰水,澄清石灰水变浑浊,说明气体中含有二氧化碳;再将气体通过灼热氧化铜,黑色固体逐渐变成红色固体,说明气体中含有一氧化碳;如果先将气体通过灼热氧化铜,反应生成的二氧化碳会影响对二氧化碳气体的检验,故选项实验方案不合理.
B、过量的BaCO3固体和稀硝酸反应生成硝酸钡、水和二氧化碳,再过滤除去过量的BaCO3固体,能除去杂质且没有引入新的杂质,符合除杂原则,故选项实验方案合理.
C、CO2和HCl气体均能与NaOH溶液反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项实验方案不合理.
D、氢氧化钠溶液与稀盐酸反应生成氯化钠和水,由于稀盐酸是少量的,加入的稀盐酸被氢氧化钠溶液反应掉,再放少量氧化铜,与氯化钠、氢氧化钠溶液均不反应,不能验证氢氧化钠和盐酸是否反应,故选项实验方案不合理.
故选:B.
点评 本题难度不是很大,化学实验方案的设计是考查学生能力的主要类型,同时也是实验教与学难点,在具体设计时要对其原理透彻理解,可根据物质的物理性质和化学性质结合实验目的进行分析判断.

练习册系列答案
相关题目
5. Ga2S3(硫化镓)是制作二维超薄半导体的材料之一.如图分别是硫元素和镓元素在元素周期表中的信息,以及硫原子的原子结构示意图.下列说法错误的是( )
Ga2S3(硫化镓)是制作二维超薄半导体的材料之一.如图分别是硫元素和镓元素在元素周期表中的信息,以及硫原子的原子结构示意图.下列说法错误的是( )
 Ga2S3(硫化镓)是制作二维超薄半导体的材料之一.如图分别是硫元素和镓元素在元素周期表中的信息,以及硫原子的原子结构示意图.下列说法错误的是( )
Ga2S3(硫化镓)是制作二维超薄半导体的材料之一.如图分别是硫元素和镓元素在元素周期表中的信息,以及硫原子的原子结构示意图.下列说法错误的是( )| A. | 硫元素属于非金属元素 | B. | x=6 | ||
| C. | 镓原子的质子数是16 | D. | 硫元素的相对原子质量为32.06 |
6.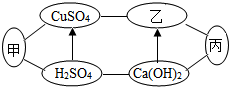 如图中甲、乙、丙是初中化学中常见的物质,图中“-”表示相连的物质之间可以在溶液中发生化学反应,“→”表示由某种物质可转化为另一种物质(部分反应物、生成物及反应条件已略去).下列说法中不正确的是( )
如图中甲、乙、丙是初中化学中常见的物质,图中“-”表示相连的物质之间可以在溶液中发生化学反应,“→”表示由某种物质可转化为另一种物质(部分反应物、生成物及反应条件已略去).下列说法中不正确的是( )
 如图中甲、乙、丙是初中化学中常见的物质,图中“-”表示相连的物质之间可以在溶液中发生化学反应,“→”表示由某种物质可转化为另一种物质(部分反应物、生成物及反应条件已略去).下列说法中不正确的是( )
如图中甲、乙、丙是初中化学中常见的物质,图中“-”表示相连的物质之间可以在溶液中发生化学反应,“→”表示由某种物质可转化为另一种物质(部分反应物、生成物及反应条件已略去).下列说法中不正确的是( )| A. | 甲、乙、丙可能依次为Fe、NaOH、CO2 | |
| B. | 当乙为NaOH时,它由Ca(OH)2与Na2CO3反应生成 | |
| C. | 甲物质只能是碱或盐 | |
| D. | 当甲为一种碱时,它与硫酸铜溶液的反应可能产生两种沉淀 |
7.不加其它试剂,利用互相反应能鉴别出来的一组是( )
| A. | FeCl3、NaOH、HCl、KCl | B. | HCl、KNO3、Na2CO3、Na2SO4 | ||
| C. | AgNO3、HCl、NaCl、HNO3 | D. | BaCl2、Na2SO4、Na2CO3、HCl |
5.化学学习让我们有了很多收获,下列归纳总结完全正确的一组是( )
| A、认识物质俗名 | B、注意实验安全 |
| ①生石灰-氧化钙 ②氢氧化钠-纯碱 | ①点燃可燃性气体前一定要验纯 ②鉴别化学药品时可以品尝 |
| C、合理利用资源 | D、健康生活方式 |
| ①随意大量使用塑料袋 ②钢铁表面刷上油漆,防止钢铁生锈 | ①平衡膳食,不偏食挑食 ②不购买食用过期食品 |
| A. | A | B. | B | C. | C | D. | D |

 2016年10月合肥第一条轻轨即将建成,如图是合肥轻轨样车图.
2016年10月合肥第一条轻轨即将建成,如图是合肥轻轨样车图.