题目内容
3.化学与生活密切相关.(1)中国的高铁技术属于国际领先地位.
①高铁轨道建设需要用大量钢筋混凝土.钢筋混凝土属于复合材料.
②高铁座椅内填充有聚氨酯软质泡沫.聚氨酯属于c(填字母).
a.金属材料 b.无机非金属材料 c.有机高分子材料
(2)营养均有利于身体健康.
①人体内提供能量的主要营养物质为油脂、糖类和蛋白质.淀粉在人体内变成葡萄糖后直接参与新陈代谢.
②维生素C能预防坏血病.如图为某品牌维生素C泡腾片说明书的部分内容.泡腾片溶于水时产生“沸腾”效果,是由于添加的酒石酸和碳酸氢钠 反应释放出了气体.

(3)煤炭在我国能源结构中占有重要地位,合理使用有利于社会可持续发展.
①控制燃煤产生的SO2排放,能够减少硫酸型酸雨的形成.燃煤排放的烟气中还含有其他污染物,请列举一种:可吸入颗粒.
②燃煤产生的CO2用NH3处理可生产多种化工产品.用氨水吸收CO2可制得碳铵(NH4HCO3),写出该反应的化学方程式CO2+H2O+NH3=NH4HCO3.用液氨与CO2反应可制备尿素[CO(NH2)2].尿素和碳铵这两种氮肥中,氮元素的质量分数较高的是尿素.
③煤的气化和液化是实现能源清洁化的重要途径.水煤气中CO和H2在加热、加压和催化剂存在条件下可以合成液体燃料(CH3OH),该反应的化学方程式为CO+2H2$\frac{\underline{\;\;\;催化剂\;\;\;}}{高温高压}$CH3OH.
分析 (1)根据材料的分类进行分析;
(2)①根据油脂、糖类和蛋白质是基本营养物质,淀粉水解生成葡萄糖进行分析;
②根据维生素C的生理功能,酒石酸呈酸性进行分析;
(3)①煤中含有硫元素,燃烧时会生成二氧化硫;
②氨气、二氧化碳、水反应生成碳酸氢铵;根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%进行分析;
③CO和H2在加热和催化剂条件下反应,可以制得液体燃料甲醇.
解答 解:(1)①钢筋混凝土是由钢筋和粘土混合而成的,是复合材料;故填:复合;
②聚氨酯属于高分子合成材料,是有机高分子化合物,故填:c;
(2)①人体内提供能量的主要营养物质为油脂、糖类和蛋白质;淀粉水解最终生成葡萄糖;故填:油脂;葡萄糖;
②维生素C能预防坏血病;酒石酸和碳酸氢钠反应释放出了气体,故填:坏血病;碳酸氢钠;
(3)①煤中含有硫元素,燃烧时会生成二氧化硫,二氧化硫被氧化为三氧化硫,三氧化硫溶于水生成硫酸,二氧化硫气体排放到空气中会形成硫酸型酸雨,煤不完全燃烧还生成可吸入颗粒,故填:硫酸;可吸入颗粒;
②氨气、二氧化碳、水反应生成碳酸氢铵:CO2+H2O+NH3=NH4HCO3;尿素的相对分子质量为60,尿素中氮元素的质量分数是$\frac{14×2}{60}$×100%≈46.7%;
碳铵的相对分子质量为:$\frac{14}{79}$×100%=17.7%,所以氮元素的质量分数较高的是尿素,故填:CO2+H2O+NH3=NH4HCO3;尿素;
③CO和H2在加热和催化剂条件下反应,可以制得液体燃料甲醇(CH3OH),故方程式为:CO+2H2$\frac{\underline{\;\;\;催化剂\;\;\;}}{高温高压}$CH3OH,故填:CO+2H2$\frac{\underline{\;\;\;催化剂\;\;\;}}{高温高压}$CH3OH.
点评 化学来源于生产、生活,也服务于生产、生活,与生产、生活相关的化学知识,关乎我们的生存、健康和社会的发展,是中考热点之一.

 阅读快车系列答案
阅读快车系列答案| A. | 有机物都含碳元素,所以含碳元素的化合物都是有机物 | |
| B. | 单质是由一种元素组成的,所以一种元素只能组成一种单质 | |
| C. | 铵盐能与碱反应产生氨气,所以硝酸铵能与氢氧化钠反应放出氨气 | |
| D. | 酸中一定含有氢元素,所以含有氢元素的物质一定是酸 |
| A. | 石蜡熔化 | B. | 钢铁生锈 | C. | 玻璃破碎 | D. | 酒精挥发 |
| A. | 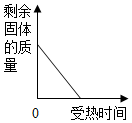 高温煅烧石灰石 | |
| B. | 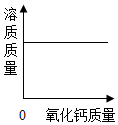 向一定温度下的饱和氢氧化钙溶液中不断加入氧化钙固体 | |
| C. | 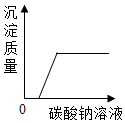 向盐酸和氯化钙的混合溶液中加入碳酸钠溶液 | |
| D. | 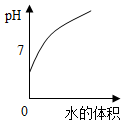 向pH=1的酸溶液中不断加水 |
| A. | 要检验混合气体中含有CO和CO2:先将气体通过灼热氧化铜,再通过澄清石灰水 | |
| B. | 除去Ba(NO3)2溶液中的HNO3:加入过量的BaCO3固体,过滤 | |
| C. | 除去CO2中的HCl气体和H2O:将混合气体依次通过足量NaOH溶液和浓H2SO4 | |
| D. | 验证氢氧化钠和盐酸反应:先向氢氧化钠溶液中加少量稀盐酸,再放少量氧化铜 |
| A. | 汽油挥发 | B. | 石墨导电 | C. | 铁钉生锈 | D. | 菜刀切菜 |