题目内容
1.物质除杂是科学实验中经常遇到的问题.某同学设计了除去氯化镁粉末中混有少量杂质的两种方法.请根据要求完成填空.(1)除去氯化镁粉末中混有的少量氯化钡,先加足量的水溶液,再向溶液中加入适量的硫酸镁溶液,过滤、蒸发,即得氯化镁固体.
(2)除去氯化镁粉末中混有的少量氯化钡、氯化钠和硫酸钾.方法如图:

滤液C中一定含有的阴离子是氯离子和氢氧根离子;
步骤③中乙溶液是HCl(填化学式)溶液.
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:(1)除去氯化镁粉末中混有的少量氯化钡,即除去钡离子,先加足量的水溶液,再向溶液中加入适量的硫酸镁溶液,硫酸镁能与氯化钡反应生成硫酸钡沉淀和氯化镁,再过滤、蒸发,即得氯化镁固体.
(2)除去氯化镁粉末中混有的少量氯化钡、氯化钠和硫酸钾,先加足量的水溶解、过滤,硫酸钾能与氯化钡溶液反应生成硫酸钡沉淀和氯化钾,过滤,滤液是氯化钠、氯化镁、氯化钾的混合溶液,向滤液中加入过量的氢氧化钠溶液,氯化镁能与氢氧化钠溶液反应生成氢氧化镁沉淀和氯化钠,则滤液C中一定含有的阴离子是氯离子和氢氧根离子;滤渣D为氢氧化镁,与稀盐酸反应生成氯化镁和水,步骤③中乙溶液是盐酸,其化学式为:HCl.
故答案为:(1)硫酸镁;(2)氯离子和氢氧根离子;HCl.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
 学习实践园地系列答案
学习实践园地系列答案
相关题目
3.某化学兴趣小组为了测定某黄铜(铜、锌合金)样品中锌的质量分数,取10g 样品放入烧杯中,再取60g 稀硫酸分六次加入烧杯中,至充分反应,实验数据如下:
(1)黄铜样品中锌的质量分数为多少?
(2)所用稀硫酸的质量分数为多少?
| 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | 第六次 | |
| 加入稀硫酸的质量(g) | 10 | 10 | 10 | 10 | 10 | 10 |
| 剩余固体的质量(g) | 9.35 | 8.7 | 8.05 | 7.4 | 6.75 | 6.75 |
(2)所用稀硫酸的质量分数为多少?
13.下列物质,与Fe2O3、BaCl2、Na2CO3均能发生反应的是( )
| A. | 水 | B. | 澄清石灰水 | C. | 稀硫酸 | D. | 硫酸钠溶液 |
11.下列关于溶液、溶解度的说法中,错误的是( )
| A. | 不饱和溶液转化为饱和溶液,溶液中溶质的质量分数可能保持不变 | |
| B. | 温度降低时,原饱和溶液可能不析出晶体 | |
| C. | 温度一定时,硝酸钾的溶解度及硝酸钾的饱和溶液中溶质的质量分数各有一定值 | |
| D. | 某溶液析出晶体后,溶液中溶质的质量分数一定减小 |
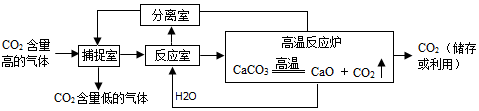
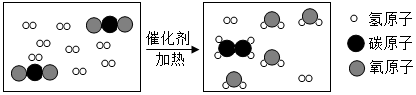
 金丽温高速铁路于2016年1月10日正式通车营运,标志着丽水进入了高铁时代,高速铁路铺设的是无缝钢轨,钢铁的主要成分是铁,铁有多种氧化物,请回答:
金丽温高速铁路于2016年1月10日正式通车营运,标志着丽水进入了高铁时代,高速铁路铺设的是无缝钢轨,钢铁的主要成分是铁,铁有多种氧化物,请回答: 某化学兴趣小组的同学为测定石灰石样品中碳酸钙的含量(杂质不溶于水也不溶于酸),同学们取石灰石样品16克,放入68.4克盐酸中,恰好完全反应,测得物质总质量的变化如图所示,求:
某化学兴趣小组的同学为测定石灰石样品中碳酸钙的含量(杂质不溶于水也不溶于酸),同学们取石灰石样品16克,放入68.4克盐酸中,恰好完全反应,测得物质总质量的变化如图所示,求: