题目内容
9.酸与碱之间发生中和反应,其实质是酸溶液中大量自由移动的H+和碱溶液中大量自由移动的OH-结合成水分子的过程.请根据以下氢氧化钠溶液与稀盐酸反应的实验,回答问题.【实验1】用酚酞试液
(1)向一锥形瓶中倾倒20g质量分数为4.00%的氢氧化钠溶液,滴入3滴酚酞试液,振荡,再逐滴滴入质量分数为3.65%的稀盐酸,边滴边振荡,直至溶液刚好变为无色为止,共用去稀盐酸20g,则反应后溶液中大量存在的微粒有Na+Cl-H2O,其溶质质量分数为2.9%(结果精确到0.1%).反应后溶液中的溶质可用蒸发的方法(填一操作名称)使其析出.用酚酞作指示剂可逐滴控制酸、碱溶液反应的量,视觉效果灵敏,操作简便.
【实验2】用pH试纸
(2)向一支试管内倒入约2mL氢氧化钠溶液,再逐滴滴入盐酸,边滴边振荡.然后用玻璃棒蘸取反应液沾到pH试纸上,与标准比色卡对照.因无法通过肉眼观察到反应进程,需间隔数滴多次检测溶液的pH,所以每使用玻璃棒蘸取溶液前,必须进行洗净擦干的预处理.
分析 氢氧化钠与盐酸反应生成的氯化钠可以通过蒸发的方法使其析出,用PH试纸测定溶液的PH,使用的玻璃棒必须保证洁净.
解答 解:(1)氢氧化钠和盐酸恰好完全反应时溶液呈中性,酚酞恰好变为无色,所得溶液为氯化钠溶液,溶液中大量存在的微粒有Na+ Cl- H2O,设生成氯化钠的质量为x,则有
NaOH+HCl=NaCl+H2O
40 58.5
20g×4.00% x
$\frac{40}{20g×4.00%}$=$\frac{58.5}{x}$
x=1.17g
所以反应后溶液中溶质质量分数为:$\frac{1.17g}{20g+20g}$×100%=2.9%,
要使氯化钠析出,可以使用蒸发的方法,所以本题答案为:无,Na+ Cl- H2O,2.9%,蒸发结晶(或蒸发);
(2)使用的玻璃棒必须保证洁净,所以本题答案为:洗净并擦干
故答案为:(1)无 Na+ Cl- H2O,2.9% (结果精确到0.1%).蒸发(2)洗净擦干
点评 本题考查了氢氧化钠与盐酸的中和反应,完成此题,可以依据已有的知识进行.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
19.随着气温回暖,云龙湖景区十里杏花竞相开放,再加上迎春、金钟的映衬,风景格外优美,吸引了众多游人,下列有关说法错误的是( )
| A. | 园林养护改浇灌为喷灌、滴灌,节约了宝贵的淡水资源 | |
| B. | 种花、种草要施一些KNO3,KNO3属于钾肥 | |
| C. | 杏花和迎春花有着不同的香味,是因为不同的分子性质不同 | |
| D. | 游人照相对,相机中的锂电池把化学能转化为电能 |
4.在一个密闭容器内有X、Y、Z、Q四种物质,在一定条件下充分反应,测得反应前后物质质量如下:
处理数据后得出的结论错误的是( )
| 物质 | X | Y | Z | Q |
| 反应前质量/g | 5 | 2 | 20 | 22 |
| 反应后质量/g | 待测 | 11 | 28 | 5 |
| A. | 反应类型为分解反应 | B. | X可能是该反应的催化剂 | ||
| C. | Y、Z变化的质量比是9:8 | D. | 反应后X的质量为0g |
14.在反应4A+5B═4C+6D中,C、D的相对分子质量之比为15:9.若6.8克A与B完全反应后,生成10.8克D.则反应中,B和D的相对分子质量比为( )
| A. | 9:16 | B. | 5:6 | C. | 16:9 | D. | 5:3 |
1.如图是甲、乙两种固体物质的溶解度曲线,下列说法正确的是( )
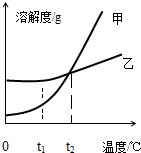

| A. | 甲物质的溶解度一定大于乙物质的溶解度 | |
| B. | 将甲溶液从t2℃降温到t1℃时,一定有晶体析出 | |
| C. | t2℃时,甲、乙饱和溶液的溶质质量分数相等 | |
| D. | 将t2℃时乙的饱和溶液变为不饱和溶液,可采用降温的方法 |
19.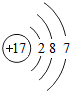 如图是元素X的原子结构示意图.下列说法正确的是( )
如图是元素X的原子结构示意图.下列说法正确的是( )
 如图是元素X的原子结构示意图.下列说法正确的是( )
如图是元素X的原子结构示意图.下列说法正确的是( )| A. | X属于金属元素 | |
| B. | 该原子核外电子数为7 | |
| C. | 该原子形成的离子可表示为X- | |
| D. | 该原子形成的离子,核外有两个电子层 |
