题目内容
14.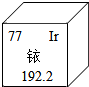 2014年5月7日在南京丢失的放射源铱-192,于5月10日安全回收.铱-192是高危放射源,会危害人体健康.如图所示是元素周期表中的一格,有关说法错误的是( )
2014年5月7日在南京丢失的放射源铱-192,于5月10日安全回收.铱-192是高危放射源,会危害人体健康.如图所示是元素周期表中的一格,有关说法错误的是( )| A. | 铱元素是金属元素 | |
| B. | 铱-192原子的质子数为77,中子数为115 | |
| C. | 铱元素的相对原子质量为192.2g | |
| D. | 铱-192和铱-191、铱-193属于同位素原子 |
分析 根据图中元素周期表可以获得的信息:左上角的数字表示原子序数;字母表示该元素的元素符号;中间的汉字表示元素名称;汉字下面的数字表示相对原子质量,进行分析判断即可.
解答 解:A.根据铱元素的汉字名称“铱”的偏旁“金”可知,为金属元素,故说法正确;
B.铱-192原子的质子数为77,中子数=相对原子质量-质子数=192-77=115,故说法正确;
C.根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,元素的相对原子质量为192.2,相对原子质量单位是“1”,不是“g”,故选项说法错误;
D.铱-192和铱-191、铱-193质子数都是77,中子数不同,属于同位素原子,故说法正确;
故选C.
点评 本题考查学生对元素周期表中元素信息的理解与在解题中应用的能力.

练习册系列答案
相关题目
7.对下列事实的解释正确的是( )
| 选项 | 事 实 | 解 释 |
| ① | 5毫升水和5毫升酒精混合后体积小于10毫升 | 分子的体积很小 |
| ② | NaOH溶液、Ca(OH)2溶液均显碱性 | 溶液中都含有氢氧根离子 |
| ③ | O2和O3的化学性质不同 | 构成物质的分子不同 |
| ④ | 浓硫酸能干燥气体 | 浓硫酸具有脱水性 |
| A. | ①②④ | B. | ②③④ | C. | ②④ | D. | ②③ |
2.要证明Zn、Cu、Ag三种金属的活动性顺序,可选用的一组试剂是( )
| A. | Zn、CuSO4溶液、AgNO3溶液 | B. | Cu、Zn、AgNO3溶液 | ||
| C. | Ag、ZnSO4溶液、CuSO4溶液 | D. | Zn、Ag、CuSO4溶液 |
6. 为证明由三种金属组成的混合粉末中,Fe和Cu的存在并测定其中Al的质量分数,某科学兴趣小组的同学展开了下列的实验探究.查阅资料得:Al与氢氧化钠溶液反应生成溶于水的偏铝酸钠和氢气(反应的化学方程式为:2Al+2H2O+2NaOH=2NaAlO2+3H2↑),Fe和Cu不与氢氧化钠溶液反应.
为证明由三种金属组成的混合粉末中,Fe和Cu的存在并测定其中Al的质量分数,某科学兴趣小组的同学展开了下列的实验探究.查阅资料得:Al与氢氧化钠溶液反应生成溶于水的偏铝酸钠和氢气(反应的化学方程式为:2Al+2H2O+2NaOH=2NaAlO2+3H2↑),Fe和Cu不与氢氧化钠溶液反应.
(1)请完成证明金属粉末中存在Fe和Cu的实验设计:
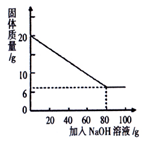
(2)为探究该金属粉末中Al的质量分数,取20g该金属粉末,加入氢氧化钠溶液反应,剩余固体质量与所加氢氧化钠溶液的质量关系如图所示,则该金属粉末中Al的质量分数为70%.
 为证明由三种金属组成的混合粉末中,Fe和Cu的存在并测定其中Al的质量分数,某科学兴趣小组的同学展开了下列的实验探究.查阅资料得:Al与氢氧化钠溶液反应生成溶于水的偏铝酸钠和氢气(反应的化学方程式为:2Al+2H2O+2NaOH=2NaAlO2+3H2↑),Fe和Cu不与氢氧化钠溶液反应.
为证明由三种金属组成的混合粉末中,Fe和Cu的存在并测定其中Al的质量分数,某科学兴趣小组的同学展开了下列的实验探究.查阅资料得:Al与氢氧化钠溶液反应生成溶于水的偏铝酸钠和氢气(反应的化学方程式为:2Al+2H2O+2NaOH=2NaAlO2+3H2↑),Fe和Cu不与氢氧化钠溶液反应.| 实验操作 | 实验现象 | 结论 |
| I.取少量的金属粉末于试管中,加入足量的氢氧化钠溶液 | 有气泡产生 | 仅除去铝 |
| II.将试管静置,弃去上层清液,加入足量的稀盐酸 | 有气泡产生 | 证明含有铁 |
| III.将试管静置,弃去上层清液,多次洗涤剩余固体 | 剩余固体 呈紫红色 | 证明含有铜 |
(2)为探究该金属粉末中Al的质量分数,取20g该金属粉末,加入氢氧化钠溶液反应,剩余固体质量与所加氢氧化钠溶液的质量关系如图所示,则该金属粉末中Al的质量分数为70%.
3.育华学校初二科学兴趣小组为了测定某矿山石灰石中碳酸钙的质量分数,取石灰石样品与足量稀盐酸在烧杯中反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水,杂质中不含钙元素)有关实验数据如下表:
(1)根据质量守恒定律可知,反应中生成二氧化碳的质量为4.4g.
(2)反应中生成氯化钙多少克?
(3)该石灰石中碳酸钙的质量分数为多少?
| 反应前 | 反应后 | ||
| 实验数据 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物的质量 |
| 150 g | 12 g | 157.6 g | |
(2)反应中生成氯化钙多少克?
(3)该石灰石中碳酸钙的质量分数为多少?

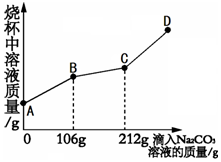 在一烧杯中盛有l00克BaCl2和HCl的混合溶液,向其中逐渐滴加溶质质量分数为10%的Na2CO3溶液,混合溶液的质量与所滴入Na2CO3溶液的质量关系曲线如图所示,请根据题意问答问题:
在一烧杯中盛有l00克BaCl2和HCl的混合溶液,向其中逐渐滴加溶质质量分数为10%的Na2CO3溶液,混合溶液的质量与所滴入Na2CO3溶液的质量关系曲线如图所示,请根据题意问答问题:
