题目内容
近来有科学家提出利用“碳捕捉技术”来降低工业生产中二氧化碳的排放量.“碳捕捉技术”是指通过一定的方法,将工业生产中产生的CO2分离出来进行储存和利用.常利用足量的NaOH溶液来“捕捉”CO2,过程如图所示(部分条件及物质未标出).
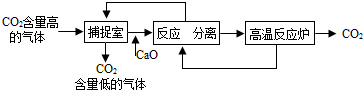
①捕捉室中发生反应的化学方程式为: .
②把CaO放入反应分离室中与H2O反应,请写出该反应的化学方程式: ;利用此反应,氧化钙可用作食品 剂.
③“反应分离”中,得到固体物质的基本操作是 ,该固体是碳酸钙.
④整个过程中,可以循环利用的物质有 .

①捕捉室中发生反应的化学方程式为:
②把CaO放入反应分离室中与H2O反应,请写出该反应的化学方程式:
③“反应分离”中,得到固体物质的基本操作是
④整个过程中,可以循环利用的物质有
考点:混合物的分离方法,过滤的原理、方法及其应用,二氧化碳的化学性质,生石灰的性质与用途,书写化学方程式、文字表达式、电离方程式
专题:物质的分离和提纯
分析:根据图示可以看出,捕捉室内是氢氧化钠和二氧化碳发生化学反应,根据反应物和生成物写出反应的化学方程式;据此解答.
解答:解:①捕捉室中氢氧化钠和二氧化碳反应生成碳酸钠和水,故填:2NaOH+CO2═Na2CO3+H2O.
②把CaO放入反应分离室中与H2O反应生成氢氧化钙;利用此反应,氧化钙可用作食品干燥剂,故填:CaO+H2O═Ca(OH)2,干燥.
③从溶液中分离得到固体物质的基本操作是过滤,故填:过滤.
④氢氧化钠与二氧化碳反应生成碳酸钠和水,氧化钙与水反应生成氢氧化钙,氢氧化钙能与碳酸钠反应生成氢氧化钠,故整个过程中,可以循环利用的物质是氢氧化钠,故填:氢氧化钠.
②把CaO放入反应分离室中与H2O反应生成氢氧化钙;利用此反应,氧化钙可用作食品干燥剂,故填:CaO+H2O═Ca(OH)2,干燥.
③从溶液中分离得到固体物质的基本操作是过滤,故填:过滤.
④氢氧化钠与二氧化碳反应生成碳酸钠和水,氧化钙与水反应生成氢氧化钙,氢氧化钙能与碳酸钠反应生成氢氧化钠,故整个过程中,可以循环利用的物质是氢氧化钠,故填:氢氧化钠.
点评:掌握常见物质的性质和物质间的反应是解答本题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案
相关题目
构成细胞的基本物质是( )
| A、蛋白质 | B、糖类 |
| C、油脂 | D、维生素 |
用浓盐酸配制一定质量分数的稀盐酸,若在用量筒量取盐酸时仰视刻度,而在量取水时俯视刻度.则所得稀盐酸中溶质的质量分数比要求配制的稀盐酸的溶质质量分数( )
| A、偏低 | B、偏高 |
| C、相同 | D、无法判断 |
有一种“即热即食型食品”适合外出旅游时使用,其内层用铝箔包装食品,外层则是包装两种化学物质.使用预留在外的开关,使两种物质发生化学反应,此时便可以对食品进行加热,这两种化学物质最适合的选择是( )
| A、熟石灰与水 | B、生石灰与水 |
| C、食盐与水 | D、浓硫酸与水 |
关于化学方程式CH4+2O2
CO2+2H2O的描述正确的是( )
| ||
| A、甲烷加氧气在点燃条件下,反应生成二氧化碳和水 |
| B、1个甲烷和2个氧气在点燃条件下,生成1个二氧化碳和2个水 |
| C、1个CH4分子和2个O2分子在点燃条件下,生成1个CO2分子和2个H2O分子 |
| D、1gCH4和2gO2在点燃条件下,生成1gCO2和2gH2O |
从水分子分解示意图中我们能获得许多信息,其中描述错误的是( )


| A、这是一个化合反应 |
| B、水分解时元素的种类不变 |
| C、在化学变化中原子是最小的粒子 |
| D、氢分子能保持氢气的化学性质 |