题目内容
13.A~I为初中化学常见的物质,它们之间的转化关系如图1所示.其中B、C、H均为气体,且C的相对分子质量比B的大16,D是人类使用量最大的金属,E的浓溶液具有强腐蚀性,F的水溶液呈蓝色.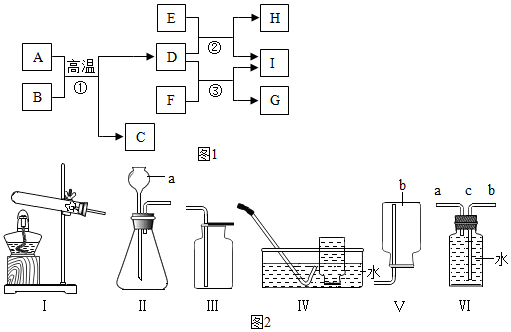
请回答:
(1)如图2所示,仪器a的名称是长颈漏斗;实验室制取C气体的化学反应方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑,常用作C气体发生装置的是Ⅱ(填装置代号),常用于收集C气体的装置是Ⅲ(填装置代号);若用装置Ⅵ收集H气体,则应从a(选填“b”或“c”)端进气.
(2)将G浸入下列溶液中,可以发生置换反应的是C(填字母).
A.MgCl2溶液 B.ZnSO4溶液 C.AgNO3溶液 D.Al2(SO4)3溶液
(3)反应③的化学方程式为Fe+CuSO4=FeSO4+Cu.
分析 根据题干提供的信息进行分析解答,D是人类使用量最大的金属,故D是铁,A和B能高温反应生成铁和气体C,故B可能是一氧化碳,C是二氧化碳,A是氧化铁,E的浓溶液具有强腐蚀性,故E是硫酸,硫酸与铁反应生成硫酸亚铁和氢气,H是氢气,I是硫酸亚铁;F的水溶液呈蓝色,能与铁反应生成硫酸亚铁,故F是硫酸铜,生成的G是铜,据此结合气体的实验室制取的知识进行分析解答即可.
解答 解:D是人类使用量最大的金属,故D是铁,A和B能高温反应生成铁和气体C,故B可能是一氧化碳,C是二氧化碳,A是氧化铁,E的浓溶液具有强腐蚀性,故E是硫酸,硫酸与铁反应生成硫酸亚铁和氢气,H是氢气,I是硫酸亚铁;F的水溶液呈蓝色,能与铁反应生成硫酸亚铁,故F是硫酸铜,生成的G是铜,带入框图,推断合理;
(1)a是长颈漏斗,C是二氧化碳,实验室使用碳酸钙和稀盐酸制取二氧化碳气体,是固液常温型反应,选择装置Ⅱ为气体的发生装置,二氧化碳的密度大于空气,能溶于水,故选择装置Ⅲ作为收集装置,用装置Ⅵ收集H气体,则是排水法收集氢气,故气体从a端进入,故填:长颈漏斗;CaCO3+2HCl═CaCl2+H2O+CO2↑;Ⅱ;Ⅲ;a;
(2)G是铜,能与硝酸银发生置换反应,故填:C;
(3)反应③是铁与硫酸铜的反应,生成硫酸亚铁和铜,故填:Fe+CuSO4=FeSO4+Cu.
点评 本题为框图式推断题,解答本题关键是要找出突破口,再根据学过的知识进一步进行分析推断即可.

练习册系列答案
 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案
相关题目
1.在一密闭容器中,有甲、乙、丙、丁四种物质,在一定条件下反应,测得反应前后各物质质量如表:
请分析该表后,回答下列问题:
(1)反应后甲的质量为3g,反应中甲物质的作用可能是催化剂.
(2)该反应中生成物为乙、丁.
(3)写出符合该反应类型的一个反应的文字表达式水$\stackrel{通电}{→}$氢气+氧气.
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 3 | 5 | 20 | 4 |
| 反应后质量/g | 待测 | 14 | 3 | 12 |
(1)反应后甲的质量为3g,反应中甲物质的作用可能是催化剂.
(2)该反应中生成物为乙、丁.
(3)写出符合该反应类型的一个反应的文字表达式水$\stackrel{通电}{→}$氢气+氧气.
8.实验操作的规范是实验的基本要求.如图实验操作正确的是( )
| A. |  过滤 | B. |  测定溶液pH | C. |  稀释浓硫酸 | D. |  闻气味 |
5.实验中学同学开展了如下“溶液酸碱性的检验”的实验活动,根据图1、图2回答下列问题:

(1)把自制的紫色紫薯汁按图1所示分别滴加到试管中,观察到的现象如表所示:
①据上表推测,紫薯汁能做酸碱指示剂,遇到稀硫酸溶液可能显示的颜色是红色,
②若将盐酸逐滴滴入滴有紫薯汁的石灰水中直至过量,你看到的溶液颜色变化过程是溶液由绿色变为紫色,最后变为红色,发生反应的化学方程式为Ca(OH)2+2HCl=CaCl2+2H2O;
(2)图2是三位同学分别测定土壤酸碱度的操作示意图,可能导致所测溶液pH数值发生改变的错误操作是(填“A”、“B”或“C”,下同)C.

(1)把自制的紫色紫薯汁按图1所示分别滴加到试管中,观察到的现象如表所示:
| 溶液 | 白醋 | 盐酸 | 食盐水 | 草木灰水 | 石灰水 |
| 加入紫薯汁后的颜色 | 红色 | 红色 | 紫色 | 绿色 | 绿色 |
②若将盐酸逐滴滴入滴有紫薯汁的石灰水中直至过量,你看到的溶液颜色变化过程是溶液由绿色变为紫色,最后变为红色,发生反应的化学方程式为Ca(OH)2+2HCl=CaCl2+2H2O;
(2)图2是三位同学分别测定土壤酸碱度的操作示意图,可能导致所测溶液pH数值发生改变的错误操作是(填“A”、“B”或“C”,下同)C.
3.下列各种物质的用途中,主要利用了其化学性质的是( )
| A. | 活性炭用于净水 | B. | 钨用于制灯泡中的灯丝 | ||
| C. | 氧气用于医疗急救 | D. | 干冰用于人工降雨 |

 某氯化钡样品中混有少量氯化钠,为测定样品中氯化钡的质量分数,将30g样品溶解于98.7g水中,再向所得溶液中滴加10.6%的碳酸钠溶液,所加碳酸钠溶液质量与生成沉淀质量的关系如图,求(结果保留一位小数):
某氯化钡样品中混有少量氯化钠,为测定样品中氯化钡的质量分数,将30g样品溶解于98.7g水中,再向所得溶液中滴加10.6%的碳酸钠溶液,所加碳酸钠溶液质量与生成沉淀质量的关系如图,求(结果保留一位小数):