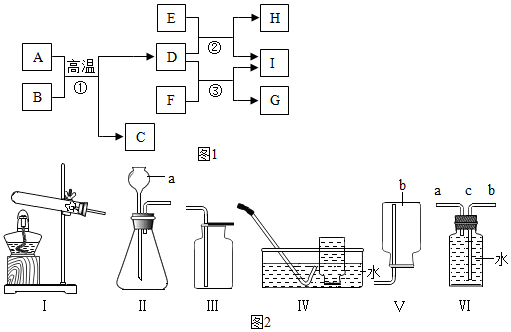
题目内容
1.在一密闭容器中,有甲、乙、丙、丁四种物质,在一定条件下反应,测得反应前后各物质质量如表:| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 3 | 5 | 20 | 4 |
| 反应后质量/g | 待测 | 14 | 3 | 12 |
(1)反应后甲的质量为3g,反应中甲物质的作用可能是催化剂.
(2)该反应中生成物为乙、丁.
(3)写出符合该反应类型的一个反应的文字表达式水$\stackrel{通电}{→}$氢气+氧气.
分析 反应后质量增加的物质是生成物,反应后质量减少的物质是反应物,反应前后质量不变的物质可能是催化剂,据此结合质量守恒定律分析解答即可.
解答 解:(1)反应后,丙的质量减少,所以是反应物,参加反应的丙的质量为:20g-3g=17g;乙、丁的质量增加,所以乙、丁是生成物,生成乙的质量为:14g-5g=9g.生成丁的质量为:12g-4g=8g;由质量守恒定律可知,甲的质量不变,故待测=3;该反应可表示为:丙→乙+丁,是由一种物质反应生成两种物质的化学反应,属于分解反应;
故填:3;催化剂;
(2)由(1)的分析可知,丙的质量减少,所以是反应物,乙、丁的质量增加,所以乙、丁是生成物,故填:乙、丁;
化合;4;
(3)该反应可表示为:丙→乙+丁,是由一种物质反应生成两种物质的化学反应,属于分解反应;故填:水$\stackrel{通电}{→}$氢气+氧气.
点评 解答这类题关键是要会运用质量守恒定律的含义:参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和.

练习册系列答案
相关题目
11.现有一包Cu(OH)2和CuO的混合粉末,加入到150g9.8%的稀硫酸中,恰好完全反应,得到163.8g溶液,则原混合粉末中Cu(OH)2和CuO的质量比为( )
| A. | 1:2 | B. | 49:20 | C. | 2:1 | D. | 40:49 |
9.类推是学习中常用的思维方法,现有以下类推结果,其中正确的是( )
| A. | 酸的溶液通常呈酸性,所以呈酸性的溶液一定是酸的溶液 | |
| B. | 氧化物都含有氧元素,所以含氧元素的化合物一定是氧化物 | |
| C. | 单质是由同种元素组成的,则由同种元素组成的物质一定是单质 | |
| D. | 化合物是由不同元素组成的纯净物,所以只含一种元素的物质不是化合物 |
16.下列属于复合肥的是( )
| A. | (NH4)2SO4 | B. | Ca3(PO4)2 | C. | KNO3 | D. | K2CO3 |
6.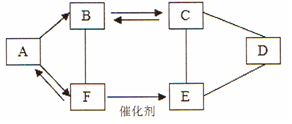 A-F为初中化学常见的六种物质,且都含有一种相同元素,他们相互间的关系如图所示.
A-F为初中化学常见的六种物质,且都含有一种相同元素,他们相互间的关系如图所示.
已知A、B、C、D、E是不同类别的物质,C俗称纯碱,F是人体中含量最多的物质(部分反应物、生成物及反应条件已略去).
下列关于A-F的说法错误的是( )
 A-F为初中化学常见的六种物质,且都含有一种相同元素,他们相互间的关系如图所示.
A-F为初中化学常见的六种物质,且都含有一种相同元素,他们相互间的关系如图所示.已知A、B、C、D、E是不同类别的物质,C俗称纯碱,F是人体中含量最多的物质(部分反应物、生成物及反应条件已略去).
下列关于A-F的说法错误的是( )
| A. | B和F均属于氧化物 | |
| B. | B物质的一种用途是人工降雨 | |
| C. | C与E正反应会生成一种白色沉淀 | |
| D. | 图中物质相互间发生的反应未涉及的基本反应类型是化合反应 |
11.根据如表数据,回答问题.
(1)20℃时,氯化钠的溶解度是36.0g;
(2)60℃时,200g硝酸钾溶液中含溶质100g,将该溶液降温至20℃,可析出硝酸钾68.4g;
(3)将等质量的氯化钠和硝酸钾饱和溶液,分别从60℃降温至20℃,下列说法正确的是ac.
a.所得溶液均为饱和溶液
b.溶剂的质量KNO3>NaCl
c.溶液中溶质的质量分数KNO3<NaCl.
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
| NaCl | 25.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 | |
(2)60℃时,200g硝酸钾溶液中含溶质100g,将该溶液降温至20℃,可析出硝酸钾68.4g;
(3)将等质量的氯化钠和硝酸钾饱和溶液,分别从60℃降温至20℃,下列说法正确的是ac.
a.所得溶液均为饱和溶液
b.溶剂的质量KNO3>NaCl
c.溶液中溶质的质量分数KNO3<NaCl.