题目内容
17.(1)生活中可用小苏打(NaHCO3)治疗胃酸过多,其反应方程式是NaHCO3+HCl═NaCl+H2O+CO2↑.(2)某同学取少量厨房清洁剂,滴入石蕊溶液后呈蓝色,说明此厨房清洁剂显碱性.
(3)外卖冰激凌中放入干冰可以使其不易融化,干冰的化学式是CO2.
分析 (1)小苏打的化学式为NaHCO3,它的水溶液呈碱性,胃酸的主要成分为氯化氢,故二者反应,发生复分解反应,其特征:两种化合物反应生成另外的两种化合物;
(2)根据已有的酸碱指示剂的知识进行分析解答;
(3)固态的二氧化碳俗称干冰.
解答 解:(1)用小苏打治疗胃酸过多,小苏打为NaHCO3,胃酸的主要成分为氯化氢,故其反应方程式是:NaHCO3+HCl═NaCl+H2O+CO2↑;
(2)某同学取少量厨房清洁剂,滴入石蕊溶液后呈蓝色,说明此厨房清洁剂显碱性;
(3)外卖冰激凌中放入干冰可以使其不易融化,干冰的化学式是CO2.
故答案为:
(1)NaHCO3+HCl═NaCl+H2O+CO2↑;
(2)碱性;
(3)CO2.
点评 本题属基础题,比较简单.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
7.下列叙述与对应的示意图表示正确的是( )
| A. | 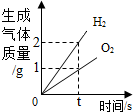 水的电解 | |
| B. | 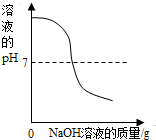 向稀盐酸中滴加过量的氢氧化钠溶液 | |
| C. | 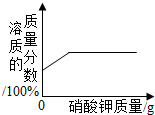 在某温度下,向一定质量的硝酸钾饱和溶液中不断加入硝酸钾晶体 | |
| D. | 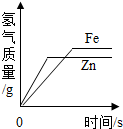 等质量的锌、铁分别与足量等溶质质量分数的稀硫酸反应 |
12.下列变化中,不属于化学变化的是( )
| A. | 葡萄酿酒 | B. | 榨西瓜汁 | C. | 食物腐败 | D. | 煤气中毒 |
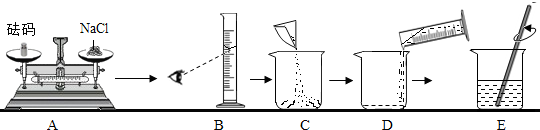
18.用如图操作可完成甲、乙两个实验,甲实验为粗盐中难溶性杂质的去除,乙实验为配制溶质的质量分数为16%的氯化钠溶液.下列说法正确的是( )
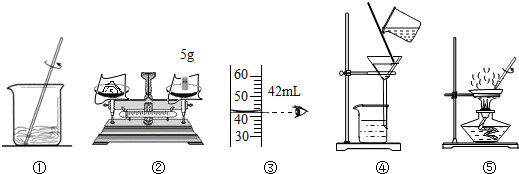

| A. | 甲实验的步骤是①④⑤,其中去除杂质的关键一步是蒸发 | |
| B. | 乙实验按照②③①的步骤进行操作,会导致配制的溶液浓度偏小 | |
| C. | 甲实验各步操作中的玻璃棒都是用来搅拌的 | |
| D. | 乙实验中,若①所用烧杯刚用清水洗过,其他步骤均正确,则配制的溶液浓度偏大 |
19.生活中某些物质的pH近似为:苹果汁3.1、泡菜3.4、西瓜汁5.8、鸡蛋清7.6,其中碱性最强的是( )
| A. | 苹果汁 | B. | 泡菜 | C. | 西瓜汁 | D. | 鸡蛋清 |