题目内容
8.在实验课上,老师要同学们配制15%的氯化钠溶液50g.(1)计算:配制15%的氯化钠溶液50g,需氯化钠的质量为7.5g.
(2)甲同学按如图所示步骤依次操作.其错误的操作步骤有AB(填字母序号);B中仪器名称为量筒;E中玻璃棒的作用是搅拌,加速溶解.
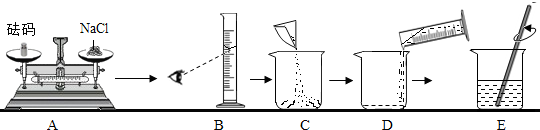
(3)乙同学在将称量好的氯化钠倒入烧杯中时,不小心有一部分氯化钠固体撒出,则其所配溶液溶质质量分数与15%相比偏低(填“偏低”、“偏高”、或“相等”)
分析 (1)根据溶质质量=溶液质量×溶质的质量分数,进行分析解答.
(2)根据托盘天平的使用要遵循“左物右码”的原则、量筒读数时视线要与凹液面的最低处保持水平,结合E溶解操作中玻璃棒的作用,进行分析判断;
(3)乙同学在将称量好的氯化钠倒入烧杯中时,不小心有一部分氯化钠固体撒出,会造成溶质氯化钠的质量偏小,据此进行分析解答.
解答 解:(1)溶质质量=溶液质量×溶质的质量分数,配制15%的氯化钠溶液50g,需称取氢氧化钠的质量为50g×15%=7.5g.
(2)托盘天平的使用要遵循“左物右码”的原则,A图中所示操作砝码与药品位置放反了,操作错误.
量取液体时,视线与液体的凹液面最低处保持水平,B图中仰视刻度,操作错误.
B中仪器名称为量筒;E是溶解操作,其玻璃棒的作用是搅拌,加速溶解.
(3)乙同学在将称量好的氯化钠倒入烧杯中时,不小心有一部分氯化钠固体撒出,会造成溶质氯化钠的质量偏小,则其所配溶液溶质质量分数与15%相比偏低.
故答案为:(1)7.5;(2)AB;量筒;搅拌,加速溶解;(3)偏低.
点评 本题难度不大,掌握配制溶质质量分数一定的溶液的基本步骤、注意事项(托盘天平、量筒的使用方法等)等是正确解答本题的关键

练习册系列答案
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案
相关题目
19. 某兴趣小组对鸡蛋壳的主要成分和含量进行了探究.
某兴趣小组对鸡蛋壳的主要成分和含量进行了探究.
I.定性探究
实验一:探究鸡蛋壳的主要成分
【查阅资料】鸡蛋壳中含钙元素.
【实验步骤和现象】取一些鸡蛋壳予一支洁净的试管中,加入过量稀盐酸,产生无色无气味的气体,将该气体通入澄清石灰水中,石灰水变浑浊.
【结论】
写出该气体通入澄清石灰水中的化学反应方程式Ca(OH)2+CO2═CaCO3↓+H2O
实验二:做无壳鸡蛋
【实验步骤和现象】如图所示:将一个新鲜鸡蛋放入水中,鸡蛋沉入水底.加入量浓盐酸后,鸡蛋会出现上浮、下沉、再上浮、再下沉的现象,反复多次.最后变成无壳鸡蛋.
【解释与交流】用化学和物理知识解释鸡蛋上浮、下沉多次的原因鸡蛋壳和盐酸反应生成的二氧化碳气泡附在鸡蛋壳表面,浮力大于重力,使鸡蛋上浮,鸡蛋到液面后,气泡破灭,重力大于浮力,鸡蛋又下沉.这样反复上下移动
Ⅱ.定量探究
化学兴趣小组为了测定鸡蛋壳中主要成分的含量(其它成分不溶于水也不与酸反应)做如下实验.取用2.00g鸡蛋壳样品,把20.00g稀盐酸分4次加入样品中,充分反应后过滤,取滤渣,洗涤、干燥、称量,得实验数据如下:
(1)从以上数据可知,这四次实验中,第四次样品中主要成分已完全反应.
(2)求鸡蛋壳中主要成分的含量和所用稀盐酸的溶质质量分数(写出计算过程).
(3)在上述实验所得滤液中加30.00g水,加入0.22g氢氧化钙能使溶液pH等于7.此时,所得溶液的溶质质量分数为4.4%.
(4)用36.5%的浓盐酸配制20.00g上述稀盐酸需加水的体积为16.0mL (保留一位小数).
 某兴趣小组对鸡蛋壳的主要成分和含量进行了探究.
某兴趣小组对鸡蛋壳的主要成分和含量进行了探究.I.定性探究
实验一:探究鸡蛋壳的主要成分
【查阅资料】鸡蛋壳中含钙元素.
【实验步骤和现象】取一些鸡蛋壳予一支洁净的试管中,加入过量稀盐酸,产生无色无气味的气体,将该气体通入澄清石灰水中,石灰水变浑浊.
【结论】
写出该气体通入澄清石灰水中的化学反应方程式Ca(OH)2+CO2═CaCO3↓+H2O
实验二:做无壳鸡蛋
【实验步骤和现象】如图所示:将一个新鲜鸡蛋放入水中,鸡蛋沉入水底.加入量浓盐酸后,鸡蛋会出现上浮、下沉、再上浮、再下沉的现象,反复多次.最后变成无壳鸡蛋.
【解释与交流】用化学和物理知识解释鸡蛋上浮、下沉多次的原因鸡蛋壳和盐酸反应生成的二氧化碳气泡附在鸡蛋壳表面,浮力大于重力,使鸡蛋上浮,鸡蛋到液面后,气泡破灭,重力大于浮力,鸡蛋又下沉.这样反复上下移动
Ⅱ.定量探究
化学兴趣小组为了测定鸡蛋壳中主要成分的含量(其它成分不溶于水也不与酸反应)做如下实验.取用2.00g鸡蛋壳样品,把20.00g稀盐酸分4次加入样品中,充分反应后过滤,取滤渣,洗涤、干燥、称量,得实验数据如下:
| 稀盐酸的用量 | 剩余固体的质量 |
| 第一次加入5.00g | 1.50g |
| 第二次加入5.00g | 1.00g |
| 第三次加入5.00g | 0.50g |
| 第四次加入5.00g | 0.30g |
(2)求鸡蛋壳中主要成分的含量和所用稀盐酸的溶质质量分数(写出计算过程).
(3)在上述实验所得滤液中加30.00g水,加入0.22g氢氧化钙能使溶液pH等于7.此时,所得溶液的溶质质量分数为4.4%.
(4)用36.5%的浓盐酸配制20.00g上述稀盐酸需加水的体积为16.0mL (保留一位小数).
16. 某无色溶液中大量存在的离子如图所示,其中X可能是( )
某无色溶液中大量存在的离子如图所示,其中X可能是( )
 某无色溶液中大量存在的离子如图所示,其中X可能是( )
某无色溶液中大量存在的离子如图所示,其中X可能是( )| A. | Ca2+ | B. | Fe3+ | C. | OH- | D. | CO32- |
3.下列各组药品,可用于验证锌、铁、铜三种金属活动性顺序的是( )
| A. | Zn、Cu、FeSO4溶液 | B. | Fe、ZnSO4溶液、CuSO4溶液 | ||
| C. | Cu、ZnSO4溶液、FeSO4溶液 | D. | Fe、Cu、ZnSO4溶液 |
20.一些食物近似pH值如下:牛奶6.4,苹果汁3.1,鸡蛋清7.8,葡萄汁4.0,其中酸性最强的是( )
| A. | 葡萄汁 | B. | 鸡蛋清 | C. | 牛奶 | D. | 苹果汁 |
 A~J分别为初中化学常见物质,他们的转换关系如图所示.已知A为铁锈的主要成分,E在常温下为无色液体,H的溶液呈蓝色,I是黑色固体,常温下B、D、F均为无色气体,其中B是有毒气体,J在工业上常用于玻璃、造纸、纺织和洗涤剂的生产等.(反应②④的个别生成物已略去)
A~J分别为初中化学常见物质,他们的转换关系如图所示.已知A为铁锈的主要成分,E在常温下为无色液体,H的溶液呈蓝色,I是黑色固体,常温下B、D、F均为无色气体,其中B是有毒气体,J在工业上常用于玻璃、造纸、纺织和洗涤剂的生产等.(反应②④的个别生成物已略去)