题目内容
15.生成相同质量的氧气理论上消耗高锰酸钾、氯化钾、5%的过氧化氢溶液的质量之比是多少?分析 根据氧气的质量通过方程式计算出需高锰酸钾、氯化钾和过氧化氢的质量;
解答 解:
解:可设生成的氧气都为32g,则有
2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
316 32
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
245 96
81.7 32
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
68 32
所以需质量分数为5%过氧化氢溶液的质量为$\frac{68}{5%}$=1360g
生成相同质量的氧气理论上消耗高锰酸钾、氯化钾、5%的过氧化氢溶液的质量之比是316:81.7:1360=3160:817:13600
答案:生成相同质量的氧气理论上消耗高锰酸钾、氯化钾、5%的过氧化氢溶液的质量之比是3160:817:13600
点评 根据化学反应方程式的计算的审题是非常关键的,一般是抓住“三找”;即一找化学反应方程式,二找已知量和未知量x,三找用到的相对质量关系,同时注意解题步骤和格式.

练习册系列答案
 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目
5.有X、Y、Z三种金属,其中Y能与稀硫酸反应,而X、Z不能;将Z进入X的盐溶液中,在Z的表面有X析出.下列选项符合X、Y、Z的是( )
| A. | Ag、Zn、Cu | B. | Zn、Mg、Cu | C. | Al、Ag、Zn | D. | Ag、Mg、Zn |
6.下列变化属于物理变化的是( )
| A. | 火箭发射 | B. | 节日烟火 | C. | 风力发电 | D. | 葡萄酿酒 |
10.现有X、Y、Z三种金属,将X、Y分别放入稀硫酸溶液中,结果Y表面产生氢气,X无变化,另取X放入Z的盐溶液中,结果X表面有Z析出,则X、Y、Z三种金属的活动顺序是( )
| A. | X>Y>Z | B. | Y>Z>X | C. | X>Z>Y | D. | Y>X>Z |
1.下列过程没有发生化学变化的是( )
①海水晒盐②海水制碱③海水淡化④从海水中提取镁.
①海水晒盐②海水制碱③海水淡化④从海水中提取镁.
| A. | 只有③ | B. | 只有② | C. | 只有②④ | D. | 只有①③ |

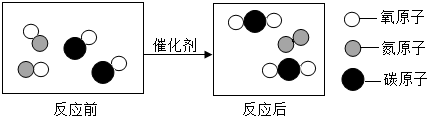 生活离不开化学,请用所学的知识解释一些问题:
生活离不开化学,请用所学的知识解释一些问题: 表示B物质的分子,B物质中碳、氧元素的质量比是3:8,6.02×1022个B分子的质量是4.4g.
表示B物质的分子,B物质中碳、氧元素的质量比是3:8,6.02×1022个B分子的质量是4.4g. 工业上炼铁的原理是利用一氧化碳和氧化铁的反应.某化学兴趣小组利用如图装置进行实验探究,请按要求填空:
工业上炼铁的原理是利用一氧化碳和氧化铁的反应.某化学兴趣小组利用如图装置进行实验探究,请按要求填空: