题目内容
10.21世纪是钛的世纪,下面是利用钛白粉(TiO2)生产海绵钛(Ti)的一种工艺流程:
(1)反应Ⅰ在800~900℃的条件下进行,生成一种无色的可燃性气体,该气体的化学式为CO.
(2)反应II可获得海锦钛,化学方程式表示为TiCl4+2Mg$\frac{\underline{\;高温\;}}{\;}$Ti+2MgCl2,该反应属于基本反应类型中的置换反应.
(3)该工艺流程中,可以循环使用的物质有镁和氯气.
分析 (1)根据质量守恒定律反应前后元素的种类不变分析生成得到气体,写出化学式;
(2)根据反应的特点分析反应的类型;
(3)根据制取钛的工艺流程图分析可循环利用的物质.
解答 解:(1)由工艺流程图及题中信息可知,反应Ⅰ的反应物为氯气、二氧化钛和焦炭,生成物为四氯化钛和一种可燃性气体,根据反应前后元素种类不变,可知此可燃性气体是由碳元素和氧元素组成的一氧化碳,化学式为CO;
(2)该反应由一种单质和一种化合物反应生成了另一种单质和另一种化合物,属于置换反应;
(2)由工艺流程图可知生成物中的镁和氯气可循环使用.
故答为:(1)CO;(2)置换;(3)镁和氯气.
点评 本题属于信息给予题,考查同学们新信息获取、处理及灵活运用所学知识(质量守恒定律,化学式、化学方程式的书写等)进行分析问题、解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.下列有关茶氨酸(化学式为C7H14O3N2)的说法中,正确的是( )
| A. | 茶氨酸属于有机高分子化合物 | |
| B. | 一个茶氨酸分子中含有一个氮分子 | |
| C. | 茶氨酸中氧元素的质量分数最大 | |
| D. | 茶氨酸中碳元素与氢元素的质量比为6:1 |
1.2015年度诺贝尔生理或医学奖获得者屠呦呦,从中药中分离出青蒿素应用于疟疾治疗.她在研究过程中发现,用低沸点溶剂提取青蒿素,药效显著提高.根据如表中物质的沸点,最适合用来冷浸法提取青蒿素的物质是( )
| 物质 | 煤油 | 丙醇 | 四氯化碳 | 乙醚 |
| 沸点/℃ | 180-310 | 97.4 | 76.5 | 34.5 |
| A. | 煤油 | B. | 丙醇 | C. | 四氯化碳 | D. | 乙醚 |
15.人类的第二杀手~心脑血管疾病,给人们的身心健康造成极大的危害.这类疾病患者大多属于酸性体质,应经常食用碱性食品.根据如表中的信息,这类患者应经常食用的食物为( )
| 食物 | 苹果 | 葡萄 | 牛奶 | 豆制品 |
| pH | 2.9-3.3 | 3.5-4.5 | 6.3-6.6 | 7.4-7.9 |
| A. | 葡萄 | B. | 苹果 | C. | 豆制品 | D. | 牛奶 |
2.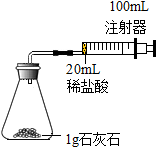 某化学实验小组对“影响石灰石与盐酸反应速率的因素--盐酸的浓度和石灰石的颗粒大小等”进行了如下实验探究,请你参与.
某化学实验小组对“影响石灰石与盐酸反应速率的因素--盐酸的浓度和石灰石的颗粒大小等”进行了如下实验探究,请你参与.
[进行实验]
室温下,选用20mL不同溶质质量分数的盐酸(4%和6%)分别与1g颗粒状或块状的石灰石进行实验(固定夹持仪器略去).
(1)石灰石与盐酸反应的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑.
(2)按上图装置进行实验,在装药品前应检查该装置的气密性,具体的做法是将注射器活塞向外拉出一段,松开手一会后,若活塞又回到原位,证明装置气密性良好.开始实验时,应将20mL稀盐酸快速(选填“快速”或“缓慢”)推入锥形瓶中,以保证盐酸能全部推入锥形瓶中.
[处理数据]
(3)实验小组进行实验后,获得的相关实验数据如表所示:
①要比较不同溶质质量分数的盐酸对反应速率的影响,可选择的实验编号是ac或是bd(写一组),由此可得到的结论是溶质质量分数越大,反应的速率越大.
②从上述实验中得出石灰石的颗粒大小反应速率影响的结论是颗粒越小,反应的速率越大.
[拓展延伸]
(4)如表是实验时记录生成的二氧化碳气体体积和对应的时间的一组实验数据(每间隔4S读数一次):
从上表数据可以分析得出,到20S后反应速率逐渐变小,其主要原因是反应物的浓度减小.
(5)你认为影响石灰石与盐酸反应速率的因素还有石灰石的纯度,请设计实验方案验证你的猜想取不同地区的石灰石,保持颗粒大小以及质量相同,加入相同的盐酸,记录生成相同的二氧化碳气体体积所需要的时间,纯度越大,速率越大.
 某化学实验小组对“影响石灰石与盐酸反应速率的因素--盐酸的浓度和石灰石的颗粒大小等”进行了如下实验探究,请你参与.
某化学实验小组对“影响石灰石与盐酸反应速率的因素--盐酸的浓度和石灰石的颗粒大小等”进行了如下实验探究,请你参与.[进行实验]
室温下,选用20mL不同溶质质量分数的盐酸(4%和6%)分别与1g颗粒状或块状的石灰石进行实验(固定夹持仪器略去).
(1)石灰石与盐酸反应的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑.
(2)按上图装置进行实验,在装药品前应检查该装置的气密性,具体的做法是将注射器活塞向外拉出一段,松开手一会后,若活塞又回到原位,证明装置气密性良好.开始实验时,应将20mL稀盐酸快速(选填“快速”或“缓慢”)推入锥形瓶中,以保证盐酸能全部推入锥形瓶中.
[处理数据]
(3)实验小组进行实验后,获得的相关实验数据如表所示:
| 实验编号 | 盐酸溶质质量分数 (均取20mL) | 石灰石固体形状 (均取1g) | 二氧化碳体积(mL) (均收集前30S的气体) |
| a | 4% | 颗粒 | 64.0 |
| b | 4% | 块状 | 40.4 |
| c | 6% | 颗粒 | 98.2 |
| d | 6% | 块状 | 65.3 |
②从上述实验中得出石灰石的颗粒大小反应速率影响的结论是颗粒越小,反应的速率越大.
[拓展延伸]
(4)如表是实验时记录生成的二氧化碳气体体积和对应的时间的一组实验数据(每间隔4S读数一次):
| 时间/S | 4 | 8 | 12 | 16 | 20 | 24 | 28 | 32 | 36 | 40 |
| 气体体积/mL | 16.0 | 22.2 | 29.4 | 39.3 | 50.4 | 57.6 | 62.0 | 64.7 | 66.0 | 66.0 |
(5)你认为影响石灰石与盐酸反应速率的因素还有石灰石的纯度,请设计实验方案验证你的猜想取不同地区的石灰石,保持颗粒大小以及质量相同,加入相同的盐酸,记录生成相同的二氧化碳气体体积所需要的时间,纯度越大,速率越大.
20. 用铱做成的钢笔尖久经耐用,价廉物美.铱在元素周期表中有关信息如图.下列说法不正确的是( )
用铱做成的钢笔尖久经耐用,价廉物美.铱在元素周期表中有关信息如图.下列说法不正确的是( )
 用铱做成的钢笔尖久经耐用,价廉物美.铱在元素周期表中有关信息如图.下列说法不正确的是( )
用铱做成的钢笔尖久经耐用,价廉物美.铱在元素周期表中有关信息如图.下列说法不正确的是( )| A. | 铱元素属于金属元素 | B. | 铱化学性质很稳定 | ||
| C. | 铱原子的核外电子数为77 | D. | 铱元素的相对原子质量为192.2g |

 化学与人体健康密切相关.
化学与人体健康密切相关.