题目内容
5.在一个密闭容器中加入四种物质,在一定条件下充分反应,测得反应前后各物质的质量如表:| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 12 | 1.2 | 2 | 5 |
| 反应后质量/g | 2 | 1.2 | x | 12 |
| A. | 甲是反应物 | B. | 测得反应后丙的质量为3g | ||
| C. | 乙一定是催化剂 | D. | 该反应是分解反应 |
分析 根据表格中的数据可知:反应后甲质量减少了12g-2g=10g,是反应物;
根据表格中的数据和质量守恒定律可知X=3g,故反应后丙质量就是3g;
反应前后乙物质质量不变,可能是催化剂,也可能既不是反应物,也不是生成物;
甲的质量减少是反应物,反应后丙物质质量增加了,是生成物,反应后丁的质量增加,是生成物,故该反应是分解反应.
解答 解:A、根据表格中的数据可知:反应后甲质量减少了12g-2g=10g,是反应物,故A正确;
B、根据表格中的数据和质量守恒定律可知,12+1.2+2+5=2+1.2+x+12,则待测x=3g,该B正确;
C、反应前后乙物质质量不变,可能是催化剂,也可能不参加反应的杂质,该C不正确;
D、甲质量减少是反应物,丙、丁的质量增加为生成物,该反应属于分解反应,该D正确;
故选:C
点评 化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变.

练习册系列答案
相关题目
13.某兴趣小组的同学进行了一系列社会调查活动,其所得结论或建议不合理的是( )
| 调查课题及内容 | 调查结论或建议 | |
| A | 使用塑料袋对环境的影响 | 减少使用并回收塑料袋,以减少污染、节约资源 |
| B | 周围人群的身体缺钙情况 | 每天服用补钙药品,而且多多益善 |
| C | 家庭用水现状 | 使用节水新技术,改变生活习惯,节约用水 |
| D | 本市一周空气质量状况 | 使用清洁能源,积极植树造林 |
| A. | A | B. | B | C. | C | D. | D |
11.下列物质在空气中敞口放置,因发生化学变化而质量增加的是( )
| A. | 浓硫酸 | B. | 浓盐酸 | C. | 氢氧化钠固体 | D. | Na2CO3•10H2O |
10.实验室用氯酸钾制取氧气,用碳酸钙和稀盐酸制取二氧化碳,下列叙述正确的是( )
| A. | 可以用同一套气体发生装置 | B. | 可以用同一种气体收集方法 | ||
| C. | 都需用到催化剂二氧化锰 | D. | 反应条件相同 |
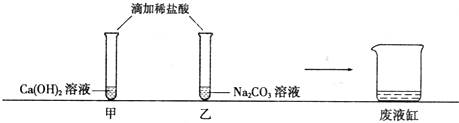
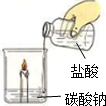 在化学学习中,我们以“透过现象看本质”的认识物质与变化.
在化学学习中,我们以“透过现象看本质”的认识物质与变化.