题目内容
14. 在化学学习中,我们以“透过现象看本质”的认识物质与变化.
在化学学习中,我们以“透过现象看本质”的认识物质与变化.(1)透过墙内开花墙外香现象,我们感受到了分子在不断运动着;
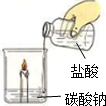
(2)根据如图实验,分析蜡烛熄灭的原因碳酸钠与盐酸反应生成了二氧化碳,使蜡烛与空气隔绝;
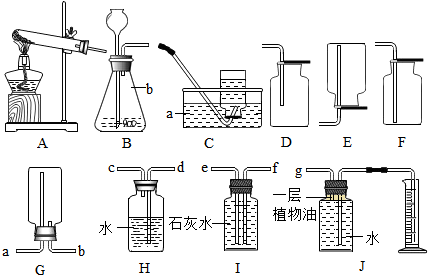
(3)通过对O2、CO2气体制取的研究,我们发现气体制取装置的选择是有规律的.如确定气体发生装置时应考虑的因素是反应物状态;反应条件;
(4)NaOH、Ca(OH)2、HCl、CO2、MgCl2五种物质间能发生的反应共有6个,根据这些反应可以归纳出碱的性质有(1)碱能和非金属氧化物发生反应(2)碱能和酸发生反应(3)碱能和盐发生反应.并写出一个放热反应对化学方程式NaOH+HCl=NaCl+H2O.
分析 根据分子运动的事例、灭火的原理气体发生装置的确定、物质的性质一一分析.
解答 解:(1)举一个分子运动的事例,能体现分子在不断的运动着;如:墙内开花墙外香;
(2)因为碳酸钠与盐酸反应生成了二氧化碳,二氧化碳的密度比空气大,会充满烧杯,使蜡烛与氧气隔绝而熄灭;
(3)制取氧气、二氧化碳选择相似的发生装置,是因为都是固液常温型,故确定气体发生装置应考虑的因素是:反应物的状态和反应条件;
(4)物质间两两混合,能发生的反应有:氢氧化钠和盐酸生成氯化钠和水;与二氧化碳生成碳酸钠和水;与氯化镁生成氯化钠和氢氧化镁;氢氧化钙和盐酸生成氯化钙和水;与二氧化碳生成碳酸钙和水;与氯化镁生成氯化钙和氢氧化镁.因此共6个反应,氢氧化钠和氢氧化钙都是碱,都能与盐酸等酸反应;与二氧化碳等非金属氧化物反应;与氯化镁等某些盐反应.
故答案为:(1)墙内开花墙外香
(2)碳酸钠与盐酸反应生成了二氧化碳,使蜡烛与空气隔绝
(3)反应物状态;反应条件
(4)6;碱能和非金属氧化物发生反应;碱能和酸发生反应;碱能和盐发生反应;NaOH+HCl=NaCl+H2O.
点评 气体发生装置的选择与反应物的状态和反应条件有关,反应物是固体和固体需要加热,反应物是固体和液体不需要加热,收集装置的选择与气体的密度和溶解性有关.

练习册系列答案
相关题目
5.在一个密闭容器中加入四种物质,在一定条件下充分反应,测得反应前后各物质的质量如表:
通过分析,判断下列说法不正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 12 | 1.2 | 2 | 5 |
| 反应后质量/g | 2 | 1.2 | x | 12 |
| A. | 甲是反应物 | B. | 测得反应后丙的质量为3g | ||
| C. | 乙一定是催化剂 | D. | 该反应是分解反应 |
2.下列各组物质中属于单质的是( )
| A. | 铁水 | B. | 水 | C. | 二氧化碳 | D. | 硫酸 |
6.下列物质中属于纯净物的是( )
| A. | 空气 | B. | 生石灰 | C. | 不锈钢 | D. | 天然气 |
3.甲、乙、丙三种不含结晶水的固体物质的溶解曲线如图所示,下列说法中正确的是( )
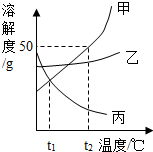

| A. | t2℃时将50g甲物质放入50g水中,充分搅拌后得到100g甲溶液 | |
| B. | t2℃时配制等质量的三种物质的饱和溶液,甲所需要的水最多 | |
| C. | 分别将t2℃时三种物质的饱和溶液降温至t1℃,所得溶液中溶质的质量分数的大小关系为乙>甲=丙 | |
| D. | 若甲溶液中有少量的乙,可用冷却热饱和溶液的方法提纯甲 |
 2015年4月6日,我省漳州古雷半岛的PX项目因装置发生漏油引发火灾事故,PX是“对二甲苯”的缩写,其组成结构如图所示,相关性质如下:
2015年4月6日,我省漳州古雷半岛的PX项目因装置发生漏油引发火灾事故,PX是“对二甲苯”的缩写,其组成结构如图所示,相关性质如下: 人类生活离不开金属.
人类生活离不开金属.