题目内容
15.现有含NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂将其转化为相应的沉淀或固体,从而实现Cl-、SO42-、和NO3-的相互分离.相应的实验过程可用下图表示:
请回答下列问题:
(1)写出实验流程中下列物质的化学式
试剂X:BaCl2 沉淀A:BaSO4 沉淀B:AaCl
(2)上述实验流程中加入过量的Na2CO3的目的是除去钡离子和银离子.
(3)按此实验方案得到的溶液3中肯定含有Na2CO3(填化学式)杂质.
分析 现有含NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂将其转化为相应的沉淀或固体,应先加入氯化钡溶液,除去硫酸根离子,再加入硝酸银除去氯离子,再加入过量的碳酸钠溶液除去钡离子和银离子,要得到硝酸钠溶液应在加入适量的稀硝酸,据此分析判断.
解答 解:由题意可知,实现Cl-、SO42-、和NO3-的相互分离,应先加入氯化钡溶液,除去硫酸根离子,再加入硝酸银除去氯离子,再加入过量的碳酸钠溶液除去钡离子和银离子,这样得到的溶液中除了氯化钠还含有碳酸钠.要得到硝酸钠溶液应在加入适量的稀硝酸,由此可知:
(1)试剂X:BaCl2 沉淀A:BaSO4 沉淀B:AaCl
(2)上述实验流程中加入过量的Na2CO3的目的是除去钡离子和银离子.
(3)按此实验方案得到的溶液3中肯定含有Na2CO3 杂质.
故答为:(1)BaCl2,BaSO4,AaCl;(2)钡离子和银离子.(3)Na2CO3.
点评 本题属于物质的提纯,在提纯除杂质的同时要注意不要引入新的杂质.

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案
相关题目
6.某实验小组的同学用碳酸钠粉末、粒状大理石、稀盐酸、浓盐酸、稀硫酸这几种药品,探究哪两种药品的反应适合在实验室制取CO2.请你参与下列的探究并回答问题.
【提出问题】上述哪两种物质的反应最适合在实验室制取CO2?
【查阅资料】1.常温下,纯净的浓盐酸是无色、有酸味和刺激性气味;它具有很强的挥发性(挥发出氯化氢气体).
2稀硫酸与碳酸钙反应,生成微溶于水的硫酸钙.
【方案设计】大家经过讨论,一致认为浓盐酸不适合用于实验室制取CO2,你认为原因浓盐酸易挥发,使制出的CO2不纯.
讨论后大家设计了如下三个实验进行对比分析.

【实验与结论】(1)请你填写实验报告中①、②处的内容.
(2)根据探究结论,实验室制取二氧化碳的反应原理为盐酸+碳酸钙─→氯化钙+水+二氧化碳 ( 用文字表达式表示).
【拓展与迁移】由上述探究可知,在确定实验室制取气体的反应原理时,要考虑诸多因素,例如反应速率要适中,便于收集等.请你再写出一种需要考虑的因素:制出的气体要纯净.
【提出问题】上述哪两种物质的反应最适合在实验室制取CO2?
【查阅资料】1.常温下,纯净的浓盐酸是无色、有酸味和刺激性气味;它具有很强的挥发性(挥发出氯化氢气体).
2稀硫酸与碳酸钙反应,生成微溶于水的硫酸钙.
【方案设计】大家经过讨论,一致认为浓盐酸不适合用于实验室制取CO2,你认为原因浓盐酸易挥发,使制出的CO2不纯.
讨论后大家设计了如下三个实验进行对比分析.

【实验与结论】(1)请你填写实验报告中①、②处的内容.
| 实验 | 实验现象 | 实验内容 |
| A | 剧烈反应,迅速放出大量气泡 | 反应速率过快,气体不便收集,不宜于实验室制取二氧化碳 |
| B | 产生气泡,速率迅速减慢,反应几乎停止. | 无法持续产生CO2,不能用于实验室制取CO2 |
| C | ①持续均匀产生气泡 | ②反应速率适中,便于收集,适合实验室制取二氧化碳 |
【拓展与迁移】由上述探究可知,在确定实验室制取气体的反应原理时,要考虑诸多因素,例如反应速率要适中,便于收集等.请你再写出一种需要考虑的因素:制出的气体要纯净.
3.下列有关说法正确的是( )
| A. | 水(H2O)由氢原子和氧原子构成的 | |
| B. | 气体受热膨胀是因为温度升高气体分子变大 | |
| C. | 化工厂可通过加高烟囱排放废气,防止大气污染 | |
| D. | 空气中含有氧分子 |
 元宵节是我国的重要传统节日,许多地方至今仍保留着燃灯放焰、共吃元宵的风俗.
元宵节是我国的重要传统节日,许多地方至今仍保留着燃灯放焰、共吃元宵的风俗. 水是人及一切生物生存所必需的,为了人类和社会经济的可持续发展,我们应该了解有关水的一些知识.请回答:
水是人及一切生物生存所必需的,为了人类和社会经济的可持续发展,我们应该了解有关水的一些知识.请回答: 实验室常采用分解H2O2的水溶液(MnO2作催化剂)的方法制取氧气.
实验室常采用分解H2O2的水溶液(MnO2作催化剂)的方法制取氧气.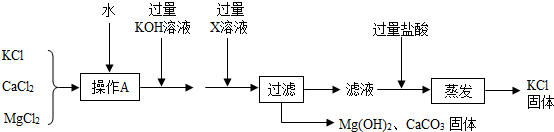
 按如图组装仪器,关闭止水夹,通电使红磷燃烧.请回答下列问题:
按如图组装仪器,关闭止水夹,通电使红磷燃烧.请回答下列问题: