题目内容
19.下列离子组能在PH=11的水溶液中大量共存的是( )| A. | Cl-、NO3-、K+、Na+ | B. | Cl-、SO42-、Na+、Ag+ | ||
| C. | SO42-、NO3-、K+、H+ | D. | Ba2+、Cl-、K+、CO32- |
分析 pH为11的水溶液显碱性,水溶液中含有大量的OH-.根据复分解反应的条件,离子间若能互相结合成沉淀、气体或水,则离子不能共存,据此进行分析判断即可.
解答 解:pH为11的水溶液显碱性,水溶液中含有大量的OH-.
A.该组离子之间不反应,能大量共存,故A正确;
B、Ag+和Cl-互相结合成氯化银沉淀,所以本组离子不能共存,故选项错误.
C、H+、OH-两种离子能结合成水,不能大量共存,故选项错误.
D、Ba2+、CO32-两种离子能结合成碳酸钡沉淀,不能大量共存,故选项错误.
故选A.
点评 本题考查离子的共存,为高考高频考点,把握复分解反应发生的条件为解答的关键,注意基础知识的考查,题目难度不大.

练习册系列答案
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案
相关题目
9.前旗六中的学生正在积极备战中考化学实验.某天当同学们再次来到实验室,意外地发现实验桌上有瓶NaOH溶液敞口放置,由此,激发了同学们的探究欲望.
【提出问题】这瓶NaOH溶液一定变质了,其变质程度如何呢?
【提出猜想】小玉的猜想:NaOH溶液部分变质;你的新猜想:全部变质.
写出氢氧化钠溶液变质的化学方程式:2NaOH+CO2═Na2CO3+H2O.
【实验探究】小玉设计如下实验来验证自己的猜想,请根据表中内容填写小玉实验时的现象
假设你的猜想正确,并按小玉的实验方案进行实验,则你观察到的实验现象是:产生白色沉淀,溶液不变色.
【实验反思】(1)下列物质①BaCl2溶液、②Ca(NO3)2溶液、③Ca(OH)2溶液、④Ba(OH)2溶液,不能替代小玉实验中CaCl2溶液的是③(填序号).
(2)小玉第二次滴加的试剂除用指示剂外,还可以用硫酸铜溶液替代.
【拓展应用】保存NaOH溶液的方法是密封保存.
【提出问题】这瓶NaOH溶液一定变质了,其变质程度如何呢?
【提出猜想】小玉的猜想:NaOH溶液部分变质;你的新猜想:全部变质.
写出氢氧化钠溶液变质的化学方程式:2NaOH+CO2═Na2CO3+H2O.
【实验探究】小玉设计如下实验来验证自己的猜想,请根据表中内容填写小玉实验时的现象
| 实验步骤 | 现 象 | 结 论 |
| 取少量NaOH溶液样品于试管中,先滴加足量的CaCl2溶液,然后再滴加酚酞试液 | 产生白色沉淀,溶液变红. | NaOH溶液部分变质 |
【实验反思】(1)下列物质①BaCl2溶液、②Ca(NO3)2溶液、③Ca(OH)2溶液、④Ba(OH)2溶液,不能替代小玉实验中CaCl2溶液的是③(填序号).
(2)小玉第二次滴加的试剂除用指示剂外,还可以用硫酸铜溶液替代.
【拓展应用】保存NaOH溶液的方法是密封保存.
10.水受热变成水蒸气时( )
| A. | 水分子变成了水蒸气的分子 | |
| B. | 水的化学性质变成水蒸气的化学性质 | |
| C. | 水分子本身没有变,水的化学性质也没有变 | |
| D. | 属于化学变化 |
7.对公共事务的决策能反映一个人的科学素养.下列有关公共事务的决策及对应的理由中,错误的是( )
| A. | 超市限制使用塑料袋--有利于减少大气污染 | |
| B. | 禁止食用野生保护动物--有利于保护生物多样性 | |
| C. | 城市推广公共自行车租赁服务--有利于减少“碳排放” | |
| D. | 对婴幼儿实施计划免疫--有助于降低婴幼儿感染传染病 |
14.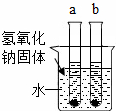 下表是a、b二种物质在不同温度时的溶解度,请根据表中数据回答:
下表是a、b二种物质在不同温度时的溶解度,请根据表中数据回答:
(1)从0℃升温到60℃,等量的水中能溶解的质量变化较小的物质是b(选填“a”或“b”).
(2)表中,20℃时物质a的溶解度是31.6克,含义是20℃时,100g水中溶解31.6g物质a正好达到饱和状态.
 下表是a、b二种物质在不同温度时的溶解度,请根据表中数据回答:
下表是a、b二种物质在不同温度时的溶解度,请根据表中数据回答:| 温度/℃ | 0 | 20 | 30 | 40 | 60 | |
| 溶解度/g | 物质a | 13.3 | 31.6 | 45.8 | 63.9 | 110 |
| 物质b | 21.4 | 9.84 | 7.24 | 5.63 | 3.87 | |
(2)表中,20℃时物质a的溶解度是31.6克,含义是20℃时,100g水中溶解31.6g物质a正好达到饱和状态.
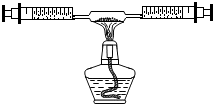 某课外活动小组在学习了书本“空气中氧气含量的测定”实验,知道P2O5不能随便排放在空气中,否则会对空气造成污染,所以对该实验进行了改进:
某课外活动小组在学习了书本“空气中氧气含量的测定”实验,知道P2O5不能随便排放在空气中,否则会对空气造成污染,所以对该实验进行了改进: