题目内容
9.前旗六中的学生正在积极备战中考化学实验.某天当同学们再次来到实验室,意外地发现实验桌上有瓶NaOH溶液敞口放置,由此,激发了同学们的探究欲望.【提出问题】这瓶NaOH溶液一定变质了,其变质程度如何呢?
【提出猜想】小玉的猜想:NaOH溶液部分变质;你的新猜想:全部变质.
写出氢氧化钠溶液变质的化学方程式:2NaOH+CO2═Na2CO3+H2O.
【实验探究】小玉设计如下实验来验证自己的猜想,请根据表中内容填写小玉实验时的现象
| 实验步骤 | 现 象 | 结 论 |
| 取少量NaOH溶液样品于试管中,先滴加足量的CaCl2溶液,然后再滴加酚酞试液 | 产生白色沉淀,溶液变红. | NaOH溶液部分变质 |
【实验反思】(1)下列物质①BaCl2溶液、②Ca(NO3)2溶液、③Ca(OH)2溶液、④Ba(OH)2溶液,不能替代小玉实验中CaCl2溶液的是③(填序号).
(2)小玉第二次滴加的试剂除用指示剂外,还可以用硫酸铜溶液替代.
【拓展应用】保存NaOH溶液的方法是密封保存.
分析 根据氢氧化钠可能全部变质,也可能是部分变质进行分析;根据氢氧化钠部分变质的成分含有氢氧化钠和碳酸钠的性质分析现象并写出反应的方程式;根据滴加的试剂和碳酸钠反应但不能产生新的碱性物质对氢氧化钠的检验产生干扰碱性分析;根据氢氧化钠的性质分析:所选择的试剂能够和氢氧化钠反应产生特殊的现象即可.
解答 解:【提出猜想】氢氧化钠可能全部变质,也可能是部分变质;故填:全部变质;
氢氧化钠能与二氧化碳反应生成碳酸钠和水,故填:2NaOH+CO2═Na2CO3+H2O;
【实验探究】氢氧化钠部分变质则含有氢氧化钠和碳酸钠两种成分,其中的碳酸钠能够和氯化钙反应产生碳酸钙白色沉淀,氢氧化钠能够使酚酞试液变成红色;故填:产生白色沉淀,溶液变红;
若氢氧化钠全部变质,则只含有碳酸钠,因此加入氯化钙会沉淀碳酸钙白色沉淀,由于没有氢氧化钠,因此滴加酚酞试液不会变成红色;故填:产生白色沉淀,溶液不变色;
【实验反思】(1)选择的试剂要求只能够和碳酸钠反应产生沉淀,既能够检验碳酸钠的存在,又能够排除碳酸钠碱性对氢氧化钠的干扰,因此不能产生新的碱性物质,氯化钡和硝酸钙都能够和碳酸钠反应产生沉淀,且没有产生碱性物质,而氢氧化钙和碳酸钠反应产生碳酸钙沉淀和氢氧化钠,因此滴加酚酞试液变成红色,不能说明是原有的氢氧化钠的作用,则不能得出部分变质的结论;故填:③;
(2)由于氢氧化钠除了能够使指示剂变色外,还能够和硫酸铜、氯化铁等产生蓝色或红褐色的测定,能够和氯化铵反应产生刺激性气味的氨气,因此可以用来检验氢氧化钠的存在.故填:硫酸铜溶液;
【拓展应用】氢氧化钠容易与二氧化碳反应,故需要密封保存,故填:密封保存.
点评 本题是有关氢氧化钠变质程度的探究,解答本题的关键是要知道变质后会变成碳酸钠,验证部分变质时要知道先把碳酸钠除掉,再验证是否含有氢氧化钠.因此熟练掌握氢氧化钠、碳酸钠的化学性质,并能够根据它们的性质来对碳酸钠及氢氧化钠进行检验.

| A. | 尾气中不可能存在O2 | B. | 尾气不可能是CO、H2 | ||
| C. | 尾气中肯定存在H2O (气)、CO2 | D. | 尾气不可能是单一气体 |
| A. | 关闭所有化工厂或搬迁至郊区 | |
| B. | 加强工地、道路和运输扬尘污染控制 | |
| C. | 研发氢能、电能等清洁能源汽车 | |
| D. | 整治烟熏腊肉、“柴火鸡”餐饮以及露天焚烧行为 |
| A. | Na2CO3、NaCl、Ba(OH)2 | B. | KCl、NaOH、CuCl2 | ||
| C. | KCl、NaOH、H2SO4 | D. | BaCl2、Na2SO4、KCl |
| A. | H2 | B. | 2N | C. | Fe | D. | CO2 |
| A. | 干冰升华 | B. | 湿衣服晒干 | ||
| C. | 自来水厂给自来水消毒 | D. | 活性炭去除冰箱异味 |
| A. | Cl-、NO3-、K+、Na+ | B. | Cl-、SO42-、Na+、Ag+ | ||
| C. | SO42-、NO3-、K+、H+ | D. | Ba2+、Cl-、K+、CO32- |
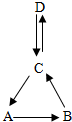 A、B、C、D均含有同一种元素,它们的转化关系如图(部分物质和反应条件已略去).
A、B、C、D均含有同一种元素,它们的转化关系如图(部分物质和反应条件已略去).