题目内容
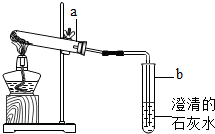
6. 小兵同学利用棉签设计了如图实验,a处滴浓氨水,b处滴酚酞溶液,过一会他观察到b处的棉花变红,a处的棉花不变红.下列说法不正确的是( )
小兵同学利用棉签设计了如图实验,a处滴浓氨水,b处滴酚酞溶液,过一会他观察到b处的棉花变红,a处的棉花不变红.下列说法不正确的是( )| A. | 氨分子在不断的运动 | |
| B. | 氨水的pH大于7 | |
| C. | 所有分子的运动速率相等 | |
| D. | 该实验药品用量少并能有效防止氨气逸出 |
分析 根据浓氨水易挥发和分子在不断的运动分析判断即可.
解答 解:A、说明氨分子在不断的运动,正确;
B、说明氨水的pH大于7,正确;
C、说明所有分子的运动速率不相等,错误;
D、该实验药品用量少并能有效防止氨气逸出,正确;
故选C.
点评 此题考查分子的定义和特性,比较简单.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.下列属于纯净物是( )
| A. | 空气 | B. | 石油 | C. | 海水 | D. | 蒸馏水 |
1.在某年的春节联欢晚会上,有一幅向观众拜年的对联是:“金银铜铁铬镍铅锌”.针对此联,下列说法正确的是( )
| A. | 这八种物质都属于金属 | |
| B. | 这八种金属均可与稀盐酸反应产生氢气 | |
| C. | 它们都是绝缘体 | |
| D. | 只用磁铁就能把这八种金属鉴别出来 |
2.属于物理变化的是( )
| A. | 鲜奶制酸奶 | B. | 干冰气化 | C. | 糯米酿甜酒 | D. | 黄豆酿酱油 |
3.下列粒子结构示意图中,表示阳离子的是( )
| A. |  | B. |  | C. |  | D. |  |