题目内容
8.现有BaCl2溶液、A溶液、B溶液,为了除NaCl溶液中混有的少量MgSO4,(1)先加入稍过量的BaCl2溶液,滤出沉淀得滤液M;(2)在滤液M中加入稍过量A溶液,滤出沉淀得滤液N;(3)在滤液N中加稍过量的B溶液,滤出沉淀后再加稍过量的C溶液加热蒸发至析出晶体.则A是氢氧化钠,B是碳酸钠,C是盐酸.分析 为了除NaCl溶液中混有的少量MgSO4,选择氯化钡除去除去硫酸根离子,选择氢氧化钠除去镁离子,选择碳酸钠除去过量的钡离子,选择氢氧化钠除去镁离子,最后加盐酸,以此来解答.
解答 解:为了除NaCl溶液中混有的少量MgSO4,(1)先加入稍过量的BaCl2溶液,除去除去硫酸根离子,滤出沉淀得滤液M为:NaCl溶液中混有的少量MgCl2以及过量的BaCl2;(2)在滤液M中加入稍过量氢氧化钠溶液,除去镁离子,滤出沉淀得滤液N为:NaCl溶液中混有的过量的BaCl2以及过量的NaOH;(3)在滤液N中加稍过量的碳酸钠溶液,除去过量的钡离子,滤出沉淀后再加稍过量的盐酸溶液除去过量的NaOH和Na2CO3,加热蒸发至析出NaCl晶体【(2)(3)步中试剂可以颠倒】.
故答案为:氢氧化钠;碳酸钠;盐酸(氢氧化钠和碳酸钠可以颠倒).
点评 本题主要考查了在粗盐提纯的实验中的除杂原则:在除去杂质的同时不能引入新的杂质.

练习册系列答案
 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
18.已知一个碳-12原子的质量为m kg,一个R原子的质量为n kg,则R原子的相对原子质量的表达式为( )
| A. | $\frac{12m}{n}$ | B. | $\frac{12n}{m}$g | C. | $\frac{12n}{m}$ | D. | $\frac{n}{12m}$ |
3.下列物质间的转化,不能一步实现的是( )
| A. | NaHCO3→CO2 | B. | KNO3→K2CO3 | C. | CO2→CaCO3 | D. | CaCO3→CaO |
11.下列现象可用质量守恒定律解释的是( )
| A. | 10g水受热变成了10g水蒸气 | |
| B. | 50mL水中加入50mL酒精,总体积小于100mL | |
| C. | 蜡烛燃烧后质量比原来减轻 | |
| D. | 5g蔗糖溶于95g水中,总质量为100g |
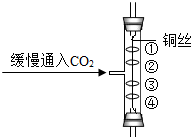 右图所示实验中,①、④为用紫色石蕊溶液润湿的棉球,②、③为用石蕊溶液染成紫色的干燥棉球.实验现象是:④比①先变红,②、③不变红.由此可得出CO2的相关性质有C
右图所示实验中,①、④为用紫色石蕊溶液润湿的棉球,②、③为用石蕊溶液染成紫色的干燥棉球.实验现象是:④比①先变红,②、③不变红.由此可得出CO2的相关性质有C