题目内容
19.序数11-17元素的符号和原子结构示意图如图所示,请结合下图回答: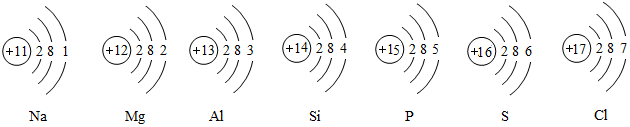
(1)原子序数为15的元素名称为磷原子的最外层有5电子;
(2)结合上图用符号表示下列内容:①原子序数为13的原子形成的离子符号Al3+,
②原子序数为12、17的元素组成化合物的化学式MgCl2.
(3)从Na-Cl,随着原子序数的增加,其原子结构(或元素的性质)呈现出的变化规律是:最外层电子数从1递增到7.(任写一条)
分析 (1)原子中,原子序数=核外电子数=核内质子数,再根据原子结构示意图,可知原子序数为15的质子数和最外层电子数;
(2)根据原子结构示意图可知:①原子序数为13的原子,最外层电子数为3个,为金属元素,易失去最外层电子,而带正电荷;②能形成双原子分子的原子为非金属元素的原子,而且可能为气态;③原子序数为12的元素的原子易失去2个电子,带2个正电荷;原子序数为17的元素的原子易得1个电子,带1个负电荷;
(3)根据原子结构示意图可知:从11-17,随着原子序数的增加,其原子结构(或元素的性质)呈现出的变化规律.
解答 解:(1)因为原子序数=核外电子数=核内质子数,所以原子序数为15的质子数为15为磷元素;根据原子结构示意图,则最外层电子数为5;
(2)根据原子结构示意图可知:
①原子序数为13的原子,最外层电子数为3个,易失去3个电子,而带3个正电荷,故离子符号为Al3+;
②原子序数为12的元素的原子易失去2个电子,带2个正电荷;原子序数为17的元素的原子易得1个电子,带1个负电荷,故原子序数为12、17的元素组成化合物的化学式MgCl2;
(3)根据原子结构示意图可知:呈现出的变化规律为:最外层电子数从1递增到7.
故答案为:(1)磷、5
(2)①Al3+;②MgCl2
(3)最外层电子数从1递增到7.
点评 本题主要考查原子结构示意图的意义,由题目给出信息,推断该元素的原子构成,对于原子构成的一些规律应当熟记;掌握化学符合及其周围的数字的意义.

练习册系列答案
相关题目
9.常温下,某气体可能是由SO2、CO、N2中的一种或几种组成,测的气体中氧元素的质量分数为50%,则该气体可能为下列组成中的( )
①SO2 ②SO2、CO ③SO2、N2 ④CO、N2 ⑤SO2、CO、N2.
①SO2 ②SO2、CO ③SO2、N2 ④CO、N2 ⑤SO2、CO、N2.
| A. | ①②③ | B. | ③③⑤ | C. | ①②⑤ | D. | ①④⑤ |
10. 某未知物质A贮存在煤油中(如图).小明为了研究这种物质,进行了实验并记录如下:
某未知物质A贮存在煤油中(如图).小明为了研究这种物质,进行了实验并记录如下:
(1)写出A物质的物理性质密度比煤油大、银白色、硬度小
(2)写出A物质的化学性质可能与空气中的气体反应.
 某未知物质A贮存在煤油中(如图).小明为了研究这种物质,进行了实验并记录如下:
某未知物质A贮存在煤油中(如图).小明为了研究这种物质,进行了实验并记录如下:| 实验内容 | 实验现象 | 结论 |
| 观察 | A沉于试剂瓶底部 | 密度比煤油的大 |
| 取出A用小刀切割 | 易切开,断面呈银白色光泽 | 硬度小、银白色 |
| 放置片刻 | 银白色变为灰暗 | 可能与空气中的气体反应 |
(2)写出A物质的化学性质可能与空气中的气体反应.
7.氨基酸是人体必需的一种营养物质,有一种氨基酸的化学式为C2H5NO2,下列有关叙述正确的是( )
| A. | 该氨基酸分子相对而言分子质量为75g | |
| B. | 该分子由两个碳元素、五个氢元素、一个氮元素、两个氧元素构成 | |
| C. | 该分子中含有NO2分子 | |
| D. | 该分子中碳、氢、氮、氧四种元素的原子个数比为2:5:1:2 |
14.观察如表,将你能得到的不同类型的结论填在横线上.(最少四点)
(1)不同原子的核内质子数不同,(2)在原子中,核内质子数=核外电子数,(3)相对原子质量=质子数+中子数,(4)有的原子不含有中子.
| 原子种类 | 质子数 | 中子数 | 电子数 | 相对原子质量 |
| 氢 | 1 | 0 | 1 | 1 |
| 氯 | 17 | 18 | 17 | 35 |
| 碳 | 6 | 8 | 6 | 14 |
| 氧 | 8 | 8 | 8 | 16 |
| 钠 | 11 | 12 | 11 | 23 |
20.下列关于催化剂的说法中正确的是( )
| A. | 一个反应只有一种催化剂 | |
| B. | 一种物质只能作一个反应的催化剂 | |
| C. | 一个反应可以有多种催化剂,它们的催化效果可能不同 | |
| D. | 催化剂在化学反应前后质量不发生变化,状态有可能改变 |
