题目内容
8.计算:(1)相同质量的钠、镁、铝三种金属,所含原子个数最多的是钠;
(2)一个碳12原子的质量为aKg,一种铁原子的质量为bKg,则该铁原子的相对原子质量为$\frac{12b}{a}$.
分析 (1)等质量的物质,所含原子个数最多,即原子质量最小;由原子的相对原子质量与其实际质量是成正比的关系,相对原子质量最小的即是原子个数最多的物质.(2)根据某原子的相对原子质量=$\frac{该元素的一个原子的质量}{一种碳原子质量×\frac{1}{12}}$,进行分析解答.
解答 解:(1)原子的相对原子质量与其实际质量是成正比,由于相对原子质量的大小关系是铝>镁>钠,真实质量也是这一关系,故1克下列各物质中,所含原子个数由多到少的顺序是:钠>镁>铝.
(2)一个碳12原子的质量为aKg,一种铁原子的质量为bKg,则该铁原子的相对原子质量为$\frac{bKg}{aKg×\frac{1}{12}}$=$\frac{12b}{a}$.
故答案为:(1)钠;(2)$\frac{12b}{a}$.
点评 本题难度不大,掌握相对原子质量与其原子真实质量成正比的关系、原子的相对原子质量=$\frac{该元素的一个原子的质量}{一种碳原子质量×\frac{1}{12}}$是正确解答本题的关键.

练习册系列答案
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案
相关题目
7.氨基酸是人体必需的一种营养物质,有一种氨基酸的化学式为C2H5NO2,下列有关叙述正确的是( )
| A. | 该氨基酸分子相对而言分子质量为75g | |
| B. | 该分子由两个碳元素、五个氢元素、一个氮元素、两个氧元素构成 | |
| C. | 该分子中含有NO2分子 | |
| D. | 该分子中碳、氢、氮、氧四种元素的原子个数比为2:5:1:2 |
3.H2和O2混合气体18g,点燃恰好完全反应,则原混合气体中H2和O2质量比是( )
| A. | 2:1 | B. | 1:8 | C. | 8:1 | D. | 无法确定 |
13.化学反应前后肯定没有变化的是( )
①分子种类②元素种类③原子种类④物质种类⑤原子数目⑥物质总质量.
①分子种类②元素种类③原子种类④物质种类⑤原子数目⑥物质总质量.
| A. | ①③④⑥ | B. | ②④⑤⑥ | C. | ②③⑤⑥ | D. | ①④⑤⑥ |
20.下列关于催化剂的说法中正确的是( )
| A. | 一个反应只有一种催化剂 | |
| B. | 一种物质只能作一个反应的催化剂 | |
| C. | 一个反应可以有多种催化剂,它们的催化效果可能不同 | |
| D. | 催化剂在化学反应前后质量不发生变化,状态有可能改变 |
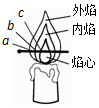 化学兴趣小组的三位同学对蜡烛(主要成分是石蜡)及其燃烧进行了如下探究.
化学兴趣小组的三位同学对蜡烛(主要成分是石蜡)及其燃烧进行了如下探究.