题目内容
18. 通过化学学习,应该知道有多种途径可以制取氧气.如:
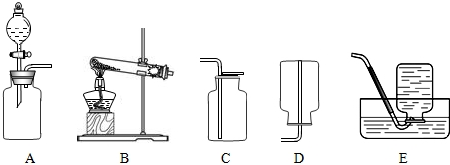
通过化学学习,应该知道有多种途径可以制取氧气.如:A.分离空气B.加热高锰酸钾 C.分解过氧化氢D.加热分解氯酸钾
(1)相信你在D处还可以写出另一种制取氧气的方法;
(2)若用右图装置加热高锰酸钾制取氧气:
写出标号仪器的名称 ①试管 ②集气瓶;
实验结束,停止加热时要先把导管移出水面,其理由是
为了防止先移走酒精灯,试管内的压强减小,水沿导管进入热的试管,使试管炸裂,
此时发现水槽中的水变成了浅紫红色,你认为产生该现象的原因可能是试管口没塞棉花;
(3)用排水法收集氧气,当气泡连续均匀冒出时,再开始收集;
(4)写出实验室加热高锰酸钾制氧气的表达式:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑
(5)过氧化氢溶液和二氧化锰混合制氧气表达式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
(6)加热氯酸钾和二氧化锰制氧气表达式:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
分析 (1)根据制取氧气的方法还有加热氯酸钾和二氧化锰混合物进行解答;
(2)根据常见仪器的名称和用途以及实验注意事项进行解答;
(3)一开始出来的气体是试管内的空气,所以开始不能收集;
(4)根据化学方程式的写法,写出化学方程式;
(5)反应物是过氧化氢,生成物是水和氧气,反应条件是二氧化锰做催化剂,用观察法配平.
(6)反应物是氯酸钾,生成物是氯化钾和氧气,二氧化锰做催化剂,用最小公倍数法配平即可.
解答 解:(1)制取氧气的方法还有加热氯酸钾和二氧化锰混合物;故答案为:加热氯酸钾和二氧化锰混合物;
(2)仪器的名称:①试管,②集气瓶;停止加热时,先把导管移出水面,再熄灭酒精灯,防止水沿着导管倒吸入试管内,使试管炸裂;试管口没有放一团棉花,加热过程中高锰酸钾颗粒进入水中,使水槽中的水变成了浅紫色;故答案为:试管;集气瓶;防止水沿着导管倒吸入试管内,使试管炸裂;试管口没有放一团棉花;
(3)一开始出来的气体是试管内的空气,所以开始不能收集,待气泡连续均匀冒出后,再进行收集;
(4)反应物是高锰酸钾,生成物是锰酸钾、二氧化锰和氧气,用观察法配平,所以方程式是:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(5)反应物是过氧化氢,生成物是水和氧气,反应条件是二氧化锰做催化剂,用观察法配平,所以方程式是:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
(6)反应物是氯酸钾,生成物是氯化钾和氧气,二氧化锰做催化剂,用最小公倍数法配平即可,所以方程式是:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
故答案:(1)D:加热分解氯酸钾
(2)①试管 ②集气瓶 为了防止先移走酒精灯,试管内的压强减小,水沿导管进入热的试管,使试管炸裂 试管口没塞棉花
(3)气泡连续均匀冒出;(4)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;(5)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;(6)2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
点评 熟记氧气的反应原理和制取装置及选取方法和注意事项;此题也考察了同学们对常用化学仪器的了解和识记情况,还应熟记化学方程式,收集氧气一般采用向上排空气法和排水法.

 名校课堂系列答案
名校课堂系列答案| A. | 金刚石 | B. | 氯化钠晶体 | C. | 氧气 | D. | 氯化钠溶液 |
 ”表示能反应,“
”表示能反应,“ ”表示不反应,则它们的金属活动性由弱到强的顺序是:( )
”表示不反应,则它们的金属活动性由弱到强的顺序是:( )| 溶液 金属 | X盐 | Y盐 |
| Zn |  |  |
| Cu |  |  |
| A. | Zn X Y Cu | B. | Cu Y Zn X | C. | Cu Y X Zn | D. | X Zn Y Cu |
| A. | 生石灰用作干燥剂 | B. | 氮气作保护气 | ||
| C. | 金刚石用作玻璃刀 | D. | 氧气用于炼钢 |
| A. | 发生火灾时用湿毛巾捂住口鼻 | |
| B. | 炒菜时油锅着火用锅盖盖灭 | |
| C. | 室内着火,逃生路线被火封住,应退回室内,关闭门窗,向门窗浇水,发出求救信号 | |
| D. | 室内燃气泄漏可以划火柴寻找泄漏点 |