题目内容
9.如图所示是初中化学常见的实验装置图,请回答: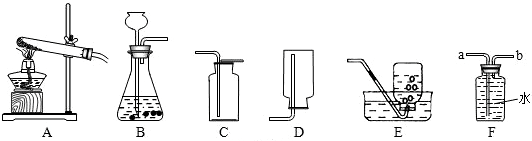
(1)实验室制取二氧化碳的方程式CaCO3+2HCl=CaCl2+H2O+CO2↑.选择的发生装置是B;收集装置是C.实验室能不能用Na2CO3与盐酸制取二氧化碳,原因是反应速率太快,不易控制.
(2)实验室用氯酸钾和二氧化锰制取氧气应选择发生装置是A; 该反应的方程式2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑; 用E装置收集氧气的原因是氧气不易溶于水;如果用F装置收集氧气,气体应从b(填a或b)进入.
分析 本题较全面地考查了氧气、二氧化碳的制取原理、装置、收集方法,解答时要认真读题,还要联想所学习的知识,再有针对性地回答.气体制备装置的选择要考虑反应物的状态和反应条件,有固固加热型和固液常温型;选择收集气体的方法时要考虑气体在水中的溶解性和气体与空气密度的相对大小,有排水集气法和向上排空气法、向下排空气法,据反应原理写出方程式.
解答 解:(1)实验室用大理石或石灰石与稀盐酸反应制取二氧化碳,发生装置应选择固液不加热装置B,二氧化碳能溶于水,密度比空气大,应选择向上排空气法C收集,发生的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
碳酸钠也能生成二氧化碳,但其反应速率太快,不易控制;
(2)实验室用氯酸钾和二氧化锰制取氧气,反应需加热,发生装置选择A;反应的方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,因氧气不易溶于水,可用排水法收集;如果用F装置收集氧气,气体应从b进入.
故答案为:(1)CaCO3+2HCl=CaCl2+H2O+CO2↑、B、C、反应速率太快,不易控制;
(2)A、2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑、氧气不易溶于水、b.
点评 本题主要考查了实验室制取氧气二氧化碳的方程式及收集方法和相关知识,是中考的重要考点.

练习册系列答案
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案
相关题目
20.以下四组离子,有一组能大量共存且能形成无色透明溶液的是( )
| A. | Fe3+ SO42- H+ Cl- | B. | H+ Na+ K+ NO3- | ||
| C. | Mg2+ Cl- OH- Na+ | D. | H+ Ba2+ NO3- SO42- |
14.下列物质属于纯净物的是( )
| A. | 清澈的海水 | B. | 冰水混合物 | C. | 洁净的空气 | D. | 自来水 |
18.有资料显示,人体含钙质量分数在1.5%左右,过多或过少都会引起病变,这里说的“钙”是指( )
| A. | 钙单质 | B. | 钙原子 | C. | 钙离子 | D. | 钙元素 |
 A、B…H 八种物质,有下图所示关系:其中A 是一种暗紫色固体,B、G 都是黑色固体,D 能使带火星的木条复燃,E 是一种无色液体,H 是一种能使澄清石灰水变浑浊的气体,在②的反应前后B的质量和化学性质都不改变.试推断:
A、B…H 八种物质,有下图所示关系:其中A 是一种暗紫色固体,B、G 都是黑色固体,D 能使带火星的木条复燃,E 是一种无色液体,H 是一种能使澄清石灰水变浑浊的气体,在②的反应前后B的质量和化学性质都不改变.试推断: