题目内容
19.新版《生活饮用水卫生标准》(简称新国标)中水质检测指标从原来的35项增加到106项,对供水各环节的水质提出了相应的要求.(1)新国标在指标中修订了镉、铅等的限量,这里的镉、铅指的是C(填序号).
A、原子 B、分子 C、元素 D、单质
(2)新国标中消毒剂由1项增至4项,加入了对用臭氧、二氧化氢和氯胺消毒的规定:
①臭氧(O3)在消毒过程中转化为氧气,臭氧转化为氧气属于化学(填“物理”或“化学”)变化.
②氯胺(NH2Cl)由三(填数字)种元素组成,用氯胺消毒时,反应的反应方程式是NH2Cl+X═NH3+HClO,其中X的化学式为H2O.
(3)净水器常用活性炭,主要是利用活性炭的吸附性,生活中,既能降低水的硬度,又能杀菌消毒的方法是煮沸.
分析 (1)根据物质的组成常用元素来描述分析;
(2)①根据变化的特征分析判断;
②由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断反应物X的化学式.
(3)根据活性炭的吸附性和生活中降低水的硬度的方法分析回答.
解答 解:(1)物质的组成常用元素来描述,新国标在指标中修订了镉、铅等的限量,这里的镉、铅指的是元素;
(2)①臭氧(O3)在消毒过程中转化为氧气,臭氧转化为氧气,有新物质生成,属于化学变化.
②一氯胺是由氮、氢和氯三种元素组成的,根据反应的化学方程式:NH2Cl+X=NH3+HClO,反应物中氮、氢、氯原子个数分别为1、2、1,反应后的生成物中氮、氢、氯、氧原子个数分别为1、4、1、1,根据反应前后原子种类、数目不变,则每个X分子由2个氢原子和1个氧原子构成,则物质X的化学式为:H2O.
(3)由于活性炭具有吸附性,净水器常用活性炭,主要是利用活性炭的吸附性,生活中,既能降低水的硬度,又能杀菌消毒的方法是煮沸.
故答案为:(1)C(2)①化学;②三;H2O.(3)吸附,煮沸.
点评 本题主要考查根据质量守恒定律推断物质的化学式和常见的净化水的方法等知识,难度较小,根据已有的知识分析解答即可.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
7.实验室有一瓶标签破损的无色溶液(如图1所示),化学兴趣小组的同学们围绕该瓶溶液的成分展开如下探究,请你一起参与.
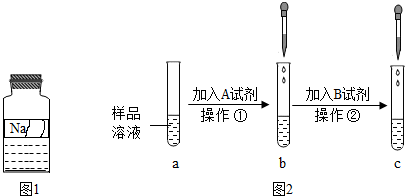
【提出问题】试剂瓶中原先存放着的药品是什么呢?
【作出猜想】试剂瓶中可能存放着氯化钠溶液、碳酸钠溶液或氢氧化钠溶液.
【设计实验】为了确定试剂瓶中原先存放的液体成分,小组同学设计了如图2所示的实验方案.
【得出结论】
实验中观察到b试管中溶液变蓝,由此得出试剂瓶中存放着的一定不是氯化钠溶液的结论,则加入的A试剂是紫色石蕊试液.通过操作②中观察到的明显现象得出试剂瓶中原先存放着碳酸钠溶液的结论,操作②中发生反应的化学方程式是Na2CO3+2HCl═2NaCl+H2O+CO2↑,c试管中一定含有的离子有Na+和Cl-.
【提出质疑】有同学对上述操作②得出的结论提出质疑,认为试剂瓶中原先存放着的液体也有可能是氢氧化钠溶液,他提出此质疑的依据是氢氧化钠能和空气中的二氧化碳反应生成碳酸钠而变质,在操作②实验中也会产生相同的现象.
【拓展探究】同学们继续设计了以下实验,确认了溶液的成分.
【实验总结】实验结束后,同学们对本次探究活动从多个角度进行了总结,请你选择一个角度说出通过本次实验活动的一条收获实验室中的许多药品都需要密封保存.

【提出问题】试剂瓶中原先存放着的药品是什么呢?
【作出猜想】试剂瓶中可能存放着氯化钠溶液、碳酸钠溶液或氢氧化钠溶液.
【设计实验】为了确定试剂瓶中原先存放的液体成分,小组同学设计了如图2所示的实验方案.
【得出结论】
实验中观察到b试管中溶液变蓝,由此得出试剂瓶中存放着的一定不是氯化钠溶液的结论,则加入的A试剂是紫色石蕊试液.通过操作②中观察到的明显现象得出试剂瓶中原先存放着碳酸钠溶液的结论,操作②中发生反应的化学方程式是Na2CO3+2HCl═2NaCl+H2O+CO2↑,c试管中一定含有的离子有Na+和Cl-.
【提出质疑】有同学对上述操作②得出的结论提出质疑,认为试剂瓶中原先存放着的液体也有可能是氢氧化钠溶液,他提出此质疑的依据是氢氧化钠能和空气中的二氧化碳反应生成碳酸钠而变质,在操作②实验中也会产生相同的现象.
【拓展探究】同学们继续设计了以下实验,确认了溶液的成分.
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量待测液于试管中,向试管中加入足量CaCl2溶液,充分反应后,再滴入无色酚酞试液 | 有白色沉淀产生,试管中液体变为红色 | 试剂瓶中原先存放着的是氢氧化钠溶液 |
14.下列说法不正确的是( )
| A. | 氧气能支持燃烧,因为氧气具有可以燃烧的性质 | |
| B. | 常用氮气做食品保护气,因为氮气的化学性质不活泼 | |
| C. | 氧气化学性质活泼,能与多种物质反应 | |
| D. | 饼干在空气中放置一段时间后会变软,说明空气中含有水蒸气 |
4.以下符号书写错误的是( )
| A. | 金刚石:C | B. | 氯化镁:MgCl2 | ||
| C. | 三个氢原子:H3 | D. | 两个硫酸根离子:2SO42- |
11.二氧化氮是大气的污染物之一.煤燃烧会产生一部分二氧化氮气体,它会与空气中的氧气、水蒸气发生反应形成酸雨,NO2+O2+H2O═HNO3,配平后各物质的化学计量数分别是( )
| A. | 1,1,1,2 | B. | 2,1,1,2 | C. | 4,1,2,4 | D. | 6,2,3,6 |
8.某校兴趣小组的同学在综合实践活动中,从水泥厂拿来一块石灰石样品,技术员告诉他们此样品中含有的杂质是二氧化硅,二氧化硅难溶于水,不能与盐酸反应.为了测定该石灰石的纯度,兴趣小组的同学取用8.00g这种石灰石样品,用实验室现有的未知溶质质量分数的稀盐酸100克分5次加入,充分反应后,经过滤、干燥等操作后称量,得到如下数据:
试回答下列问题:
(l)表中m的值为4g.杂质的质量是1.2g
(2)计算该石灰石样品的纯度.
(3)反应生成的气体质量是多少克?
| 实 验 次 数 | 1 | 2 | 3 | 4 | 5 |
| 加入稀盐酸的质量/g | 20.0 | 20.0 | 20.0 | 20.0 | 20.0 |
| 剩余固体的质量/g | 6.00 | m | 2.00 | 1.20 | 1.20 |
(l)表中m的值为4g.杂质的质量是1.2g
(2)计算该石灰石样品的纯度.
(3)反应生成的气体质量是多少克?
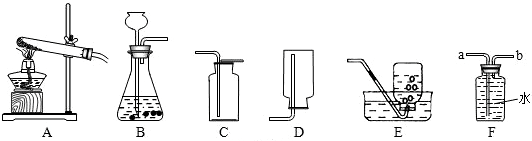
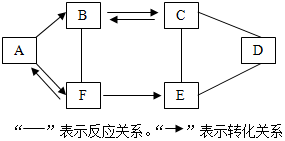 A~F为初中化学常见的六种物质,且都含有一种相同元素,它们相互间的关系如图所示.己知A、B、C、D、E是不同类别的物质,C俗称纯碱,F是人体中含量最多的物质.(部分反应物、生成物及反应条件
A~F为初中化学常见的六种物质,且都含有一种相同元素,它们相互间的关系如图所示.己知A、B、C、D、E是不同类别的物质,C俗称纯碱,F是人体中含量最多的物质.(部分反应物、生成物及反应条件