题目内容
4.酸、碱、盐均为重要的化合物.请利用所学知识完成下列问题.(1)酸和碱在组成和性质方面有很多共同的特点,请任写出其中的一条.酸和碱的组成中都含有氢元素.
(2)请写出一个既能检验烧碱变质、又能除去杂质的有关反应的化学方程式:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH.
(3)配制一定质量分数的氢氧化钠溶液,有关操作如下图所示:
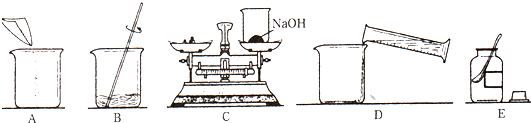
以上实验的正确操作顺序为ECADB(用字母代号表示);C操作中出现的错误天平称量物体质量应该是左物右码.
(4)用pH试纸测定所配制溶液的酸碱度,操作方法为用玻璃棒蘸取少量待测液体滴在pH试纸上,然后将试纸显示的颜色与标准比色卡对照,读出pH值.
分析 (1)根据酸在水溶液中会电离出氢离子,碱在水溶液中会电离出氢氧根离子进行分析;
(2)根据氢氧化钠变质生成碳酸钠,碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠进行分析;
(3)根据配制溶液的步骤是计算、称量、溶解、装瓶,以及天平的正确使用方法进行分析;
(4)根据用pH试纸溶液的酸碱度的方法进行分析.
解答 解:(1)酸在水溶液中会电离出氢离子,碱在水溶液中会电离出氢氧根离子,所以酸和碱在组成和性质方面共同的特点是:酸和碱的组成中都含有氢元素;
(2)氢氧化钠变质生成碳酸钠,碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,化学方程式为:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
(3)配制溶液的步骤是计算、称量、溶解、装瓶,所以正确操作顺序为ECADB,C操作中出现的错误是天平称量物体质量应该是左物右码;
(4)用pH试纸溶液的酸碱度的方法是:用玻璃棒蘸取少量待测液体滴在pH试纸上,然后将试纸显示的颜色与标准比色卡对照,读出pH值.
故答案为:(1)酸和碱的组成中都含有氢元素;
(2)Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
(3)ECADB,天平称量物体质量应该是左物右码;
(4)用玻璃棒蘸取少量待测液体滴在pH试纸上,然后将试纸显示的颜色与标准比色卡对照,读出pH值.
点评 本题主要考查了酸碱的性质、溶液的配制、pH值的测定,难度不大,需要在平时的学习中加强记忆.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
16. 如图所示的装置是测定空气中氧气的含量,对该实验认识正确的是( )
如图所示的装置是测定空气中氧气的含量,对该实验认识正确的是( )
 如图所示的装置是测定空气中氧气的含量,对该实验认识正确的是( )
如图所示的装置是测定空气中氧气的含量,对该实验认识正确的是( )| A. | 使用红磷的量多或少,都不会影响实验结果 | |
| B. | 燃烧足够的红磷可使进入容器的水占容器的$\frac{4}{5}$ | |
| C. | 红磷燃烧消耗空气中的氧气,使容器内的压强减小,水从烧杯进入容器 | |
| D. | 红磷一燃烧完,就立即观察并记录水进入容器的刻度 |
14.下列说法不正确的是( )
| A. | 氧气能支持燃烧,因为氧气具有可以燃烧的性质 | |
| B. | 常用氮气做食品保护气,因为氮气的化学性质不活泼 | |
| C. | 氧气化学性质活泼,能与多种物质反应 | |
| D. | 饼干在空气中放置一段时间后会变软,说明空气中含有水蒸气 |