题目内容
3.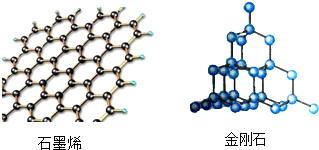 碳及其化合物广泛在于自然界中,如图是石墨烯和金刚石两种碳单质的结构模型(图中每一个球代表一个碳原子),下列有关说法正确的是( )
碳及其化合物广泛在于自然界中,如图是石墨烯和金刚石两种碳单质的结构模型(图中每一个球代表一个碳原子),下列有关说法正确的是( )| A. | 石墨烯和金刚石中的碳原子间都存在间隔 | |
| B. | 石墨烯和金刚石中的碳原子静止不动 | |
| C. | 石墨烯或金刚石在空气中燃烧只能生成一种碳的氧化物 | |
| D. | 常温下,石墨烯和金刚石的化学性质都比较活泼 |
分析 A、根据原子之间有间隔考虑;B、根据原子始终在不断运动考虑;C、根据碳燃烧的产物考虑;D、根据碳化学性质稳定考虑.
解答 解:A、原子之间有间隔,所以石墨烯和金刚石中的碳原子间都存在间隔,故A正确;
B、原子始终在不断运动,故B错;
C、碳完全燃烧生成二氧化碳,不完全燃烧生成一氧化碳,故C错;
D、碳化学性质稳定,所以常温下,石墨烯和金刚石的化学性质都比较稳定,故D错.
故选A.
点评 解答本题关键是知道原子的特点和性质,知道碳化学性质和稳定性.

练习册系列答案
相关题目
13.如表是元素周期表中部分元素的原子结构示意图,请分析:
(1)在化学反应中Mg原子易失(填“得”或“失”)电子•
(2)Na+离子核外的电子数为10;
(3)经分析发现,元素的周期数与原子的电子层数、元素的主族数与原子的最外层电子数有着密切的关系;请推断X原子的最外层电子数为3,Y原子的电子层数为4;
(4)若镓(Ga)元素与氯元素只组成一种属于盐的化合物,请写出该化合物的化学式GaCl3.
| ⅠA | ⅡA | ⅢA | |
| 第2周期 |  | 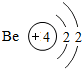 | 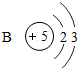 |
| 第3周期 |  |  | X |
| 第4周期 | Y | 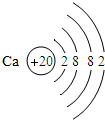 | 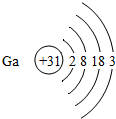 |
(2)Na+离子核外的电子数为10;
(3)经分析发现,元素的周期数与原子的电子层数、元素的主族数与原子的最外层电子数有着密切的关系;请推断X原子的最外层电子数为3,Y原子的电子层数为4;
(4)若镓(Ga)元素与氯元素只组成一种属于盐的化合物,请写出该化合物的化学式GaCl3.
14.物质的性质决定其用途.下列物质的用途与性质对应关系错误的是( )
| A. | 氢氧化钙可用来改良酸性土壤--氢氧化钙溶液呈碱性 | |
| B. | 铁粉能做食品包装中的“双吸剂”--铁在常温下能与水和氧气共同反应 | |
| C. | 固体二氧化碳可用人工降雨--二氧化碳能与水反应 | |
| D. | 氧化钙可做食品干燥剂--氧化钙能与水反应 |
11. 分析图判断关于氧元素的相关信息正确的是( )
分析图判断关于氧元素的相关信息正确的是( )
 分析图判断关于氧元素的相关信息正确的是( )
分析图判断关于氧元素的相关信息正确的是( )| A. | 氧原子的质量为16.00g | B. | 氧原子的结构示意图为 | ||
| C. | 氧为金属元素 | D. | 氧原子的质子数为8 |
18.温室效应又称“花房效应”,是大气保温效应的俗称,自工业革命以来,人类向大气中排入的二氧化碳等吸热性强的温室气体逐年增加,大气的温室效应也随之增强,其引发的一系列问题已引起了全世界的关注.下列做法不能减少温室气体的是( )
| A. | 开发风能,太阳能等清洁能源 | B. | 大量植树造林,严禁乱砍滥伐 | ||
| C. | 研究开发二氧化碳回收利用技术 | D. | 提倡家用汽车代替公交车出行 |
15.下列实验能验证质量守恒定律的是( )
| A. | 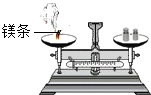 镁条在空气中燃烧前后质量的测定 | |
| B. | 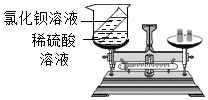 氯化钡溶液与稀硫酸溶液反应前后质量的测定 | |
| C. | 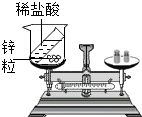 锌粒和稀盐酸反应前后质量的测定 | |
| D. | 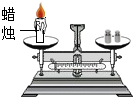 蜡烛燃烧前后质量的测定 |
12.某学校化学兴趣小组为了测定实验中高锰酸钾样品的纯度,取10g该样品进行了加热,加热的时间与剩余固体的质量关系如表所示(假设杂质不参加反应,数值看作为理论值).
(1)加热t4时间后,高锰酸钾是否已经完全反应是(填“是”或“否”).
(2)求该样品中高锰酸钾的质量分数(即纯度)(可能用到的相对原子质量:O-16,K-39,Mn-55).
| 加热时间 | t1 | t2 | t3 | t4 |
| 剩余固体质量(g) | 9.56 | 9.28 | 9.04 | 9.04 |
(2)求该样品中高锰酸钾的质量分数(即纯度)(可能用到的相对原子质量:O-16,K-39,Mn-55).
13.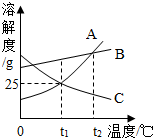 如图是A、B、C三种物质的溶解度曲线,说法错误的是( )
如图是A、B、C三种物质的溶解度曲线,说法错误的是( )
 如图是A、B、C三种物质的溶解度曲线,说法错误的是( )
如图是A、B、C三种物质的溶解度曲线,说法错误的是( )| A. | 物质A的溶解度随温度的升高而增大 | |
| B. | t1℃时,物质C饱和溶液的溶质质量分数为20% | |
| C. | 将t2℃时物质C的饱和溶液降温到t1℃时,溶液浓度变大 | |
| D. | 将t2℃时的物质A、B饱和溶液降温到t1℃时,两溶液的浓度B>A |