题目内容
12.过氧化氢溶液在二氧化锰作催化剂的条件下能迅速分解生成氧气和水.分液漏斗可以通过调节活塞控制液体的滴加速度.(如图所示)
回答下列问题:
(1)分液漏斗中应放入的物质是过氧化氢溶液,锥形瓶中应放入的物质是二氧化锰.
(2)写出该方法制取O2的符号表达式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;若要收集较为纯净的氧气,应选择的收集装置为D(填编号).做硫粉在氧气中燃烧的实验时,需在集气瓶底部放少量水的作用是吸收二氧化硫,防止污染空气,该反应的符号表达式为:S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2,该反应的基本类型为化合反应.
(3)用此方法制取O2的优点是②(填编号).
①生成物只有氧气 ②不需加热 ③需加热
(4)装置A中反应很剧烈,据此提出实验安全注意事项①(填编号).
①控制液体的滴加速度 ②用体积较小的锥形瓶 ③加热反应物.
分析 (1)通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;
(2)考虑氧气的密度比空气大,不易溶于水;根据硫在空气、氧气中燃烧的现象、发生的反应、注意事项等分析回答;
(3)考虑不同的实验方法,具有不同的优缺点;
(4)考虑反应物接触越充分,温度越高,反应速率越快.
解答 解:(1)分液漏斗中应放入的物质是过氧化氢溶液,锥形瓶中应放入的物质是二氧化锰;
(2)如果用双氧水和二氧化锰制氧气就不需要加热,加药品时要先固后液,二氧化锰放入锥形瓶中,过氧化氢溶液加入分液漏斗中,制取氧气的表达式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;硫粉在空气中燃烧火焰呈淡蓝色,而在氧气中燃烧,发出蓝紫色火焰,且生成无色有刺激性气味的气体二氧化硫.该实验集气瓶底部放少量水的目的是:吸收二氧化硫,防止污染空气;该反应的文字表达式为:S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2;该反应由两种物质生成了一种物质,属于化合反应;
故填:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑; D,吸收二氧化硫,防止污染空气,S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2,化合反应
(3)这种方法与实验室用KMnO4加热制取O2相比,优点是不需加热;
(4)装置A中反应很剧烈,据此提出实验安全注意事项是控制液体的滴加速度,不能用体积较小的锥形瓶或加热反应物,因为这样会加快反应.故填:①.
故答案为:
(1)过氧化氢溶液,二氧化锰.
(2)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑; D,吸收二氧化硫,防止污染空气,S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2,化合反应.
(3)②,(4)①.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

| A. | ②④③①⑤⑥⑦ | B. | ②④③①⑤⑦⑥ | C. | ②①③④⑤⑥⑦ | D. | ②①⑥⑦③④⑤ |
| A. | O2 | B. | CO2 | C. | N | D. | Na |
[提出问题]镁是否能与水反应?
[实验探究]在两个烧杯中,A烧杯中加入一定量的冷水和镁条,B烧杯中加入等量的热水和镁条,用酚酞指示剂.实验过程和现象如图:
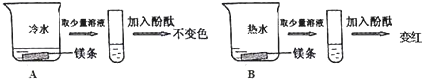
[反思与总结]
(1)小明得出的实验结论是镁不能与冷水反应,能与热水发生反应.
(2)小明发现B试管放置空气中一会儿溶液的红色会褪色,这说明溶液的碱性减弱了.于是他大胆作出了一个猜想并设计了验证方案:
| 猜想 | 验证方案 |
| 可能是氢氧化镁的溶解度受温度的影响,温度降低,溶解度变小,从而导致溶液的浓度降低,溶液的碱性减弱. | 将褪色后的溶液加热,如果溶液变红,说明小明的猜想正确. |
| A. | 电解水 | B. | 硫在氧气中燃烧 | ||
| C. | 利用过氧化氢制氧气 | D. | 二氧化碳通入澄清石灰水 |
 如图是氯元素的原子和离子结构示意图,请据图说出两者的相似点B
如图是氯元素的原子和离子结构示意图,请据图说出两者的相似点B