题目内容
3.实验室制取氧气的过程主要分以下几步:①点燃酒精灯给药品加热 ②检查装置的气密性 ③用铁夹把试管固定在铁架台上,使管口略向下倾斜 ④将氯酸钾和二氧化锰的混合物装入试管中,用带导管的胶塞塞紧 ⑤用排水法收集氧气 ⑥将导管从水槽中取出 ⑦熄灭酒精灯.正确的操作顺序是( )| A. | ②④③①⑤⑥⑦ | B. | ②④③①⑤⑦⑥ | C. | ②①③④⑤⑥⑦ | D. | ②①⑥⑦③④⑤ |
分析 根据加热氯酸钾或加热高锰酸钾分解制取氧气时,操作步骤和注意点分别是:连(连接仪器、组装实验装置)→查(检查装置的气密性)→装(装入固体药品,注意用高锰酸钾时,在试管口放一团棉花)→定(用铁架台固定仪器装置)→点(用火柴点燃酒精灯,给试管加热;注意要用外焰,先预热,再固定在有药品的部位加热)→收(收集氧气)→移(把导管移出水面)→熄(熄灭酒精灯),进行解答.
解答 解:根据实验室用加热方法制取氧气的操作步骤:连、查、装、定、点、收、移、熄,可得题中正确的操作顺序是:②④③①⑤⑥⑦;
故选A.
点评 熟记制取氧气的实验步骤、装置示意图及其中仪器的名称、注意事项等等,方能顺利解题.

练习册系列答案
相关题目
3.碳12原子的质量为1.993×10-26kg,一种铬原子的质量为8.636×10-26kg,则该铬原子的相对原子质量为( )
| A. | 4.3×10-26kg | B. | 4.3 | C. | 52.0 | D. | 52.0g |
18.下列叙述错误的是( )
| A. | 空气的成分按质量分数计算,氮气约占78%,氧气约占21% | |
| B. | 稀有气体都没有颜色,没有气味,化学性质很不活泼 | |
| C. | 空气是一种十分重要的资源 | |
| D. | 工业上分离液态空气制氧气,没发生化学变化 |
13.甲同学在探究酸的性质时,误把H2O2溶液当作酸与Fe2O3粉末混合,发现有大量气泡产生.他联想到MnO2可作为H2O2分解的催化剂,那么,Fe2O3能否作为H2O2分解的催化剂呢?请你一起参与探究,并填写下列空白.
【猜想】Fe2O3能作为H2O2分解的催化剂.
【实验验证】甲同学依次设计了三个实验:
实验一 取一定量的H2O2溶液于试管中,观察到有极少量气泡产生,伸入带火星的木条,没有复燃.说明H2O2溶液常温下缓慢分解.
实验二 在实验一的试管中加入W g Fe2O3粉末,有大量气泡产生,然后伸入带火星的木条,木条复燃.说明Fe2O3能加快H2O2的分解速率.
实验三 待反应结束后,将试管里的不溶物滤出,并洗涤、干燥、称量,固体质量仍为W g.说明反应前后Fe2O3的质量保持不变.
【实验结论】甲同学认为,Fe2O3粉末可以作为H2O2分解的催化剂.
【反思评价】乙同学认为要证明甲同学的结论正确,仅做这三个实验还不充分,需要再补充一个探究实验.探究反应前后Fe2O3的化学性质是否改变.
【拓展】下表是丙同学探究影响H2O2分解因素时所记录的部分数据,通过对数据分析,你能得出什么结论?相同条件下,MnO2的催化效果比Fe2O3好(或其他条件相同的情况下,H2O2浓度越大,产生氧气的速率越快).(任写一条)
用足量等体积H2O2溶液制取相同体积O2所需的时间:
【猜想】Fe2O3能作为H2O2分解的催化剂.
【实验验证】甲同学依次设计了三个实验:
实验一 取一定量的H2O2溶液于试管中,观察到有极少量气泡产生,伸入带火星的木条,没有复燃.说明H2O2溶液常温下缓慢分解.
实验二 在实验一的试管中加入W g Fe2O3粉末,有大量气泡产生,然后伸入带火星的木条,木条复燃.说明Fe2O3能加快H2O2的分解速率.
实验三 待反应结束后,将试管里的不溶物滤出,并洗涤、干燥、称量,固体质量仍为W g.说明反应前后Fe2O3的质量保持不变.
【实验结论】甲同学认为,Fe2O3粉末可以作为H2O2分解的催化剂.
【反思评价】乙同学认为要证明甲同学的结论正确,仅做这三个实验还不充分,需要再补充一个探究实验.探究反应前后Fe2O3的化学性质是否改变.
【拓展】下表是丙同学探究影响H2O2分解因素时所记录的部分数据,通过对数据分析,你能得出什么结论?相同条件下,MnO2的催化效果比Fe2O3好(或其他条件相同的情况下,H2O2浓度越大,产生氧气的速率越快).(任写一条)
用足量等体积H2O2溶液制取相同体积O2所需的时间:
时间(min) 浓度 催化剂 | 30%H2O2溶液 | 15%H2O2溶液 | 5%H2O2溶液 |
| 加入W g MnO2 | 0.2 | 0.8 | 2.0 |
| 加入W g Fe2O3 | 7.0 | 9.0 | 16.0 |
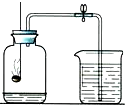 为了测定空气中氧气的含量,按如图进行实验:请通过实验现象和题中信息,按要求填空:
为了测定空气中氧气的含量,按如图进行实验:请通过实验现象和题中信息,按要求填空: 如图是测定空气中氧气含量的实验装置根据实验回答问题.
如图是测定空气中氧气含量的实验装置根据实验回答问题.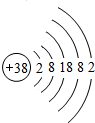 据《自然》杂志报道,科学家最近研制的一种以锶原子做钟摆的钟是世界上最精确的钟.锶元素(元素符号为Sr)原子结构示意图如图所示.
据《自然》杂志报道,科学家最近研制的一种以锶原子做钟摆的钟是世界上最精确的钟.锶元素(元素符号为Sr)原子结构示意图如图所示.