题目内容
19.过氧化钠(Na2O2)是一种供氧剂,与水反应的化学方程式为2Na2O2+2H2O═4NaOH+O2↑,将一定量的Na2O2加入到足量水中,完全反应后所得溶液的质量比原来的总质量减少了1.6g(水的挥发忽略不计),请计算:(1)生成氧气的质量为1.6g;
(2)求参加反应的过氧化钠的质量.
分析 (1)完全反应后所得溶液的质量和反应物的总质量之差,即为生成氧气的质量;
(2)根据氧气的质量可以计算反应的过氧化钠的质量;
解答 解:(1)生成氧气的质量为1.6g.
故填:1.6.
(2)设参加反应的过氧化钠的质量为x,
2Na2O2+2H2O═4NaOH+O2↑
156 32
x 1.6g
$\frac{156}{x}=\frac{32}{1.6g}$
x=7.8g,
答:参加反应的过氧化钠的质量为7.8g.
点评 本题主要考查学生运用化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
9.下列图象分别与选项中的操作相对应,其中可能合理的是( )
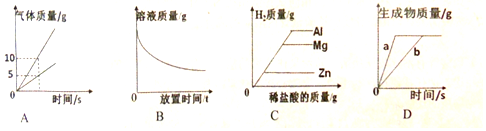

| A. | 电解水产生气体的变化 | |
| B. | 敞口放置于空气中的浓硫酸 | |
| C. | 等质量的镁、铝、锌分别与等质量等浓度的稀盐酸反应 | |
| D. | 用等质量等浓度的过氧化氢溶液制氧气,加MnO2的曲线是b |
10.下列除去杂质的方法中正确的是( )
| 选项 | 物质 | 杂质 | 除杂质的方法 |
| A | CaCl2溶液 | 稀盐酸 | 过量碳酸钙、过滤 |
| B | KOH溶液 | KCl | 适量硝酸银、过滤 |
| C | HCl溶液 | H2SO4 | 过量氢氧化钡溶液、过滤 |
| D | O2 | CO | 通过灼热的氧化铜 |
| A. | A | B. | B | C. | C | D. | D |
7.某物质在空气中完全燃烧生成4.4g二氧化碳和2.7g水,则关于这种物质的组成描述正确的是( )
| A. | 该物质的化学式可能为C2H6O | |
| B. | 该物质的分子中碳原子与氢原子的个数比为1:2 | |
| C. | 该物质只含有碳元素和氢元素 | |
| D. | 该物质中碳元素与氢元素的质量比为12:1 |
14.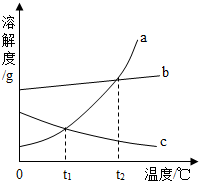 如图是a、b、c三种固体的溶解度曲线,下列说法正确的是( )
如图是a、b、c三种固体的溶解度曲线,下列说法正确的是( )
 如图是a、b、c三种固体的溶解度曲线,下列说法正确的是( )
如图是a、b、c三种固体的溶解度曲线,下列说法正确的是( )| A. | t1℃时a、c两种溶液中溶质的质量相等 | |
| B. | t2℃时质量相等的三种饱和溶液中,溶质质量最大的是c | |
| C. | 当a中含有少量b时,可以用降温结晶的方法提纯a | |
| D. | t2℃三种饱和溶液降温至t1℃,溶质质量分数大小关系为b>a=c |
17.下表是氯化钠、硝酸钾在不同温度时的溶解度.据此判断:下列说法不正确的是( )
| 温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | 氯化钠 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| 硝酸钾 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
| A. | 氯化钠和硝酸钾的溶解度曲线在20℃~30℃温度范围内会相交 | |
| B. | 在20℃时,向68g饱和氯化钠溶液中加入32g水,此时溶液中溶质的质量分数为18% | |
| C. | 从含有少量氯化钠的饱和硝酸钾溶液中得到较多的硝酸钾晶体,可采用冷却热饱和溶液使其结晶的方法 | |
| D. | 分别将20℃时一定质量的饱和氯化钠溶液、饱和硝酸钾溶液升温至40℃,此时硝酸钾溶液中溶质的质量分数大于氯化钠溶液 |
18.物质性质决定用途.下列有关物质的性质与用途的关系不正确的是( )
| A. | 钛合金与人体“相容性”好,可用于制造人造骨 | |
| B. | 铝的导电性好,密度小,所以用来当高压电缆 | |
| C. | 甲醛有防腐作用,可用于保存易腐败的食品 | |
| D. | 洗洁精有乳化作用,常用做碗筷的洗涤剂 |
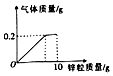 向盛有100g稀硫酸的烧杯中逐渐加入10g锌粒,产生气体质量与锌粒质量的关系如图所示.请根据关系图分析并计算:
向盛有100g稀硫酸的烧杯中逐渐加入10g锌粒,产生气体质量与锌粒质量的关系如图所示.请根据关系图分析并计算: