题目内容
9.下列图象分别与选项中的操作相对应,其中可能合理的是( )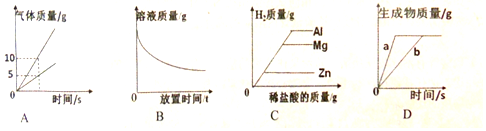
| A. | 电解水产生气体的变化 | |
| B. | 敞口放置于空气中的浓硫酸 | |
| C. | 等质量的镁、铝、锌分别与等质量等浓度的稀盐酸反应 | |
| D. | 用等质量等浓度的过氧化氢溶液制氧气,加MnO2的曲线是b |
分析 A、根据电解水的实验结论可以完成解答;
B、根据硫酸的吸水性分析;
C、根据金属与酸反应时酸的质量与氢气的关系分析;
D、根据催化剂的特点分析判断.
解答 解:A、电解水实验中产生氢气和氧气的质量之比为1:8,故A错;
B、由于浓硫酸具有吸水性,敞口放置于空气中的浓硫酸中溶剂的质量增大,溶质质量不变,故B错;
C、根据金属与酸的反应时产生氢气的质量=$\frac{金属的化合价}{金属的相对原子质量}$×金属的质量可知,等质量的镁、铝、锌分别与等质量等浓度的稀盐酸反应生成氢气的多少关系是:铝>镁>锌,故C正确;
D、由于二氧化锰能加快过氧化氢的分解,所以用等质量等浓度的过氧化氢溶液制氧气,反应的时间短,加MnO2的曲线是a,故D错.
故选C.
点评 熟练掌握酸碱盐的化学性质,能够熟练的运用金属的活动性顺序的应用来解答相关题目,知道电解水实验中氢气和氧气的体积比为2:1,而不是质量比.

练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目
19.兰州中山桥是黄河上游修建最早和唯一保存至今的近现代钢架桥梁,做桥梁的钢架属于( )
| A. | 非金属材料 | B. | 有机合成材料 | C. | 复合材料 | D. | 金属材料 |
17.以太阳能为热源,硫碘循环分解水是一种高效、无污染的制氢方法.其反应过程如图所示:
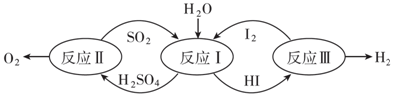
反应Ⅱ的化学方程式为2H2SO4=2SO2↑+O2↑+2H2O,它由两步反应组成:
第一步:H2SO4=SO3↑+H2O;第二步:SO3分解.
下列说法中正确的是( )

反应Ⅱ的化学方程式为2H2SO4=2SO2↑+O2↑+2H2O,它由两步反应组成:
第一步:H2SO4=SO3↑+H2O;第二步:SO3分解.
下列说法中正确的是( )
| A. | 反应Ⅰ方程式为:SO2+I2+2H2O=H2SO4+2HI | |
| B. | 反应Ⅱ中的第二步反应中,SO3分解生成S和O2 | |
| C. | 反应Ⅰ属于化合反应,反应Ⅱ、III属于分解反应 | |
| D. | 该生产工艺中最终被消耗的物质是H2O、S和I2 |
4.下列各组物质中,按照混合物、氧化物、碱的顺序排列的是( )
| A. | 加碘盐、水、纯碱 | B. | 稀有气体、干冰、熟石灰 | ||
| C. | 冰水混合物、液氧、火碱 | D. | 钢、高锰酸钾、氢氧化镁 |
1.食用纯碱的主要成分是碳酸钠,另外还含有少量的氯化钠:取13.5g样品放入烧杯中,每次加入20g稀盐酸(不考虑水、氯化氢逸出)后用精密仪器称量,记录实验数据如下:
(1)表中数据a=3.3g,b=4.95g.
(2)请你在下边的坐标纸上绘制生成气体的质量与所加稀盐酸质量关系的曲线.
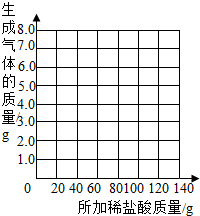
(3)计算所用稀盐酸的溶质质量分数.
| 加入盐酸的次数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 烧杯及所称物质总质量/g | 78.9 | 97.8 | 116.7 | 135.60 | 155.05 | 175.05 | 195.05 |
| 生成气体的质量/g | 1.1 | 2.2 | a | 4.4 | 4.95 | b | -- |
(2)请你在下边的坐标纸上绘制生成气体的质量与所加稀盐酸质量关系的曲线.

(3)计算所用稀盐酸的溶质质量分数.
18.下列化学用语与正确的是( )
| A. | 2个氢原子:2H | B. | 氧分子:O | C. | 铜离子:Cu2+ | D. | 硫酸钠:NaSO4 |
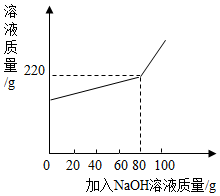 将一定量氯化镁和氯化钠的固体混合物加水配成145.8g的溶液,向所得溶液中加入一定浓度的氢氧化钠溶液,加入氢氧化钠溶液的质量与反应后溶液的质量关系如图.计算:
将一定量氯化镁和氯化钠的固体混合物加水配成145.8g的溶液,向所得溶液中加入一定浓度的氢氧化钠溶液,加入氢氧化钠溶液的质量与反应后溶液的质量关系如图.计算: