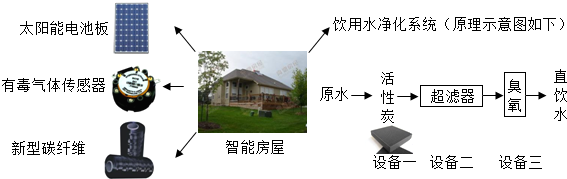
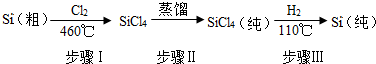
题目内容
14.某兴趣小组对物质的性质进行相关探究【提出问题】氯化氢(HCl)气体显酸性吗?
【进行实验】该兴趣小组的同学根据二氧化碳与水反应的实验探究方法,用三朵由紫甘蓝的汁液染成蓝紫色的纸质干燥小花进行如图1的三个实验:

实验现象:Ⅰ和Ⅱ中小花不变色;Ⅲ中小花变红色.
【查阅资料】图2是同学们查阅的氯化氢气体溶于水的示意图.
【实验结论】氯化氢气体不显酸性.
【交流反思】(1)从微观角度分析氯化氢气体不显酸性的原因在氯化氢气体中,氯化氢气体是由氯化氢分子构成的,没有解离出的氢离子,所以氯化氢气体不显酸性.
(2)小明向实验Ⅲ中变红的小花上喷足量的稀氢氧化钠溶液,发现小花最后变成黄绿色,写出相关反应的化学方程式NaOH+HCl═NaCl+H2O.
(3)下列实验可以用来说明氯化氢气体不显酸性的是B.
A、测试盐酸的导电性,盐酸能导电B、干燥的碳酸钠粉末放入氯化氢气体中,不反应学C、氢气与氯气反应,生成氯化氢气体D、干燥的碳酸钠粉末放入盐酸中,能反应
【拓展应用】
(4)该兴趣小组的同学为探究分子的运动情况,在玻璃管两端同时放入蘸有试剂的棉花,做了如图3所示实验,发现在玻璃管内形成了白色烟环(成分为氯化铵)且偏向蘸有浓盐酸的棉花一端.
①白色烟环偏向蘸有浓盐酸的棉花一端的原因是氨分子的运动速率大于氯化氢分子的运动速率,所以生成的白色烟环偏向蘸有浓盐酸的棉花一端.
②写出该反应的化学方程式NH3+HCl═NH4Cl.
分析 (1)根据氯化氢气体是由氯化氢分子构成的进行分析;
(2)根据题中所给的反应物、生成物以及反应条件结合质量守恒定律进行分析;
(3)根据碳酸钠粉末遇到酸性物质会生成二氧化碳进行解答;
(4)①根据影响分子运动速率的因素进行分析;
②根据反应物、生成物以及反应条件结合质量守恒定律进行解答.
解答 解:(1)氯化氢气体是由氯化氢分子构成的,没有解离出的氢离子,所以氯化氢气体不显酸性,故填:在氯化氢气体中,氯化氢气体是由氯化氢分子构成的,没有解离出的氢离子,所以氯化氢气体不显酸性;
(2)氢氧化钠溶液和盐酸反应生成氯化钠和水,所以向实验Ⅲ中变红的小花上喷足量的稀氢氧化钠溶液,发现小花最后变成黄绿色,反应的化学方程式为:NaOH+HCl═NaCl+H2O;
(3)碳酸钠粉末遇到酸性物质会生成二氧化碳,所以干燥的碳酸钠粉末放入氯化氢气体中,不反应,说明氯化氢气体不显酸性,故填:B;
(4)①相对分子质量越大,分子的运动速率越慢,相对分子质量越小,分子的运动速率越快,氨气的相对分子质量小于氯化氢的相对分子质量,所以氨分子的运动速率大于氯化氢分子的运动速率,所以生成的白色烟环偏向蘸有浓盐酸的棉花一端,所以填:氨分子的运动速率大于氯化氢分子的运动速率,所以生成的白色烟环偏向蘸有浓盐酸的棉花一端;
②在常温下,氨气和氯化氢气体反应生成氯化铵固体,该反应的化学方程式:NH3+HCl═NH4Cl;
故答案为:(1)在氯化氢气体中,氯化氢气体是由氯化氢分子构成的,没有解离出的氢离子,所以氯化氢气体不显酸性;
(2)NaOH+HCl═NaCl+H2O;
(3)B;
(4)①氨分子的运动速率大于氯化氢分子的运动速率,所以生成的白色烟环偏向蘸有浓盐酸的棉花一端;
②NH3+HCl═NH4Cl.
点评 在解此类题时,首先要了解题中的各个问题,然后将这些问题对准学过的知识点,再结合题中的要求各个突破.

 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案| A. | s=$\frac{100m}{a-m}$克 | B. | s=$\frac{100(m-{m}_{1})}{a-b}$克 | ||
| C. | s=$\frac{100({m}_{1}-{m}_{2})}{b-c}$克 | D. | s=$\frac{100{m}_{2}}{c}$克 |


 如图所示是硫原子的结构示意图.
如图所示是硫原子的结构示意图.