题目内容
2.研究和控制化学反应条件有重要意义.(1)同学们想探究双氧水的浓度对反应速率的影响.在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间.
| 实验 | 30%双氧水的质量(g) | 加入的水的体积(mL) | 二氧化锰质量(g) | 收集时间(s) |
| 1 | 20 | 40 | 5 | 200 |
| 2 | 20 | 30 | 5 | 100 |
| 3 | 20 | 20 | -- | 67 |
②上述实验结束后可用过滤的方法来分离二氧化锰和水的混合物.
③实验3中,加入的二氧化锰质量为5g,反应中二氧化锰作催化剂.
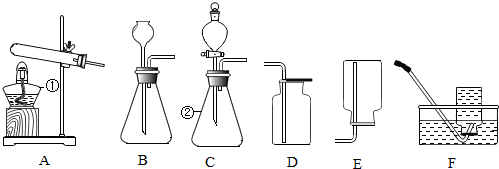
④实验中要记录收集一瓶氧气所需的时间,收集时应该选用图1装置中的B.

(2)同学通过查阅资料得知,双氧水在70℃以上会较快分解产生氧气.为了验证加热双氧水也可以产生氧气,同学们选择图2装置(气密性良好)进行实验.实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是氧气中混有较多的水蒸气,同学分析原因后经过改进,再进行检验,证明加热双氧水也可产生氧气.
分析 (1)①根据双氧水在二氧化锰催化作用下生成水和氧气写出反应的方程式;
②根据二氧化锰不溶于水来分析;
③实验是探究双氧水的溶质质量分数对反应速率的影响.在其他条件相同的情况下进行了三次实验;
④根据该实验需要观察收集一瓶气体所用的时间,进行分析所选用的收集方法.
(2)根据在加热双氧水的过程中一定会有水蒸气散出,使收集的氧气不纯及收集纯净气体的方法分析.
解答 解:(1)①过氧化氢在二氧化锰的催化作用下生成水和氧气,反应的方程式是:2H2O2$\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2↑;故填:2H2O2$\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2↑;
②二氧化锰是一种不溶于水的固体粉末,可用过滤的方法加以分离;故填:过滤;
③实验探究双氧水的溶质质量分数对反应速率的影响.所以在其他条件相同的情况下进行了三次实验,所以实验3中,加入的二氧化锰质量为5g;其中二氧化锰做催化剂;故填:5;催化剂;
④该实验需要观察收集一瓶气体所用的时间,用排水法容易准确地判断收集满氧气的时间.故填:B;
(2)在加热双氧水的过程中一定会有水蒸气散出,使收集的氧气不纯,所以将带火星的木条放在导管口没有复燃;故答案为:氧气中混有较多的水蒸气.
点评 本题考查了实验装置的选择、气体收集装置的选择、化学方程式的书写等知识,考查的范围较大,需要同学们细心分析解答.

练习册系列答案
 华东师大版一课一练系列答案
华东师大版一课一练系列答案
相关题目
12.下列现象或事实,用分子、原子的相关知识加以解释,其中不正确的是( )
| 选项 | 现象或事实 | 解释 |
| A | 稀有气体可作保护气 | 原子核外电子达到相对稳定结构 |
| B | 物质热胀冷缩 | 分子大小随温度改变而改变 |
| C | 氧气和臭氧(O3)性质不完全相同 | 构成物质的分子不同 |
| D | 氧化汞受热分解为汞和氧气 | 在化学变化中分子可以再分 |
| A. | A | B. | B | C. | C | D. | D |
17.化学与我们生活生产息息相关.下列说法或解释不正确的是( )
| A. | 焚烧秸秆会严重污染空气,主要因为秸秆燃烧产生大量有害气体和烟尘 | |
| B. | 许多食品会与氧气发生反应而变质,故在包装时可以充入氮气作为保护气 | |
| C. | 工厂的污水会严重污染河流,可以注入地下来治理 | |
| D. | 农业上需水量很大,采取滴灌的方式可以提高水的利用效益 |
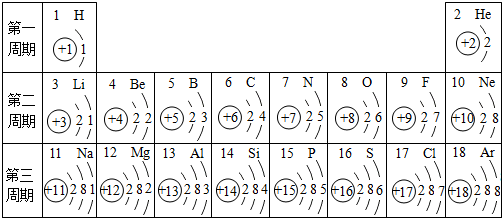

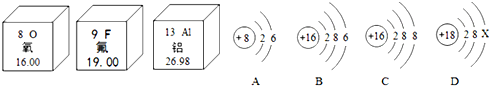
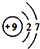 ,氟原子在化学反应中易得到(填“得到”或
,氟原子在化学反应中易得到(填“得到”或 根据下列图片及文字回答问题:
根据下列图片及文字回答问题: