题目内容
某化学兴趣小组的同学利用下图实验对碳酸钙高温加热,一段时间,发现石灰水变浑浊,停止加热,同学们对剩余固体的成分进行探究.
【提出问题】加热后剩余固体的成分是什么?
【提出猜想】
猜想一:碳酸钙全部分解,剩余固体成分为 ,
做出该猜想的依据是(用化学方程式表示) .
猜想二:碳酸钙部分分解,剩余固体成分为 .
【方案与结论】
| 实验步骤 | 实验现象 | 实验结论 | |
| 步骤1 | 将少量剩余固体放入盛有水的烧杯中,搅拌、静置,滴加少量酚酞 |
| 猜想二成立 |
| 步骤2 | 向步骤1中的烧杯中滴加盐酸至过量 |
|

【考点】实验探究物质的组成成分以及含量;生石灰的性质与用途;盐的化学性质;书写化学方程式、文字表达式、电离方程式.
【专题】科学探究.
【分析】根据物质的性质进行分析,碳酸钙高温能分解生成氧化钙和二氧化碳,氧化钙能与水反应生成氢氧化钙,氢氧化钙是微溶于水的物质,其水溶液呈碱性,碳酸钙能与盐酸反应生成二氧化碳气体.
【解答】解:猜想一:碳酸钙能分解生成氧化钙和二氧化碳,若碳酸钙全部分解,则剩余的固体时氧化钙,故填:氧化钙,CaCO3 CaO+CO2↑;
CaO+CO2↑;
猜想二:若碳酸钙部分分解,则所剩余的固体中含有氧化钙和碳酸钙,固体:氧化钙、碳酸钙,
【方案与结论】氧化钙能与水反应生成氢氧化钙,氢氧化钙是微溶于水的物质,其水溶液呈碱性,能使酚酞试液变红,故观察到溶液变红,可以证明固体中含有氧化钙,碳酸钙能与盐酸反应生成气体,故可以采用加入盐酸,观察到有气体产生,证明猜想二正确,
| 实验步骤 | 实验现象 | 实验结论 | |
| 步骤1 | 将少量剩余固体放入盛有水的烧杯中,搅拌、静置,滴加少量酚酞 | 烧杯中液体变 | 猜想二成立 |
| 步骤2 | 向步骤1中的烧杯中滴加盐酸至 | 液体由红色变无色,有气泡产生 |
故答案为:CaO(或氧化钙);CaCO3 CaO+CO2↑;氧化钙、碳酸钙;
CaO+CO2↑;氧化钙、碳酸钙;
【方案与结论】
烧杯中液体变红;液体由红色变无色,有气泡产生.
【点评】本题考查了物质变质成分的探究,完成此题,可以依据已有的物质的性质进行.要求同学们熟练掌握常见物质的性质,以便灵活应用.

 通城学典默写能手系列答案
通城学典默写能手系列答案某校同学开展了如图所示“溶液酸碱性的检验”的实验活动.

①把自制的紫色紫薯汁按图1所示分别滴加到试管中,观察到的现象如下表所示:
| 溶液 | 白醋 | 盐酸 | 食盐水 | 草木灰水 | 石灰水 |
| 加入紫薯汁后的颜色 | 红色 | 红色 | 紫色 | 绿色 | 绿色 |
由表可知,紫薯汁能做酸碱指示剂,若遇到稀硫酸溶液显示的颜色是 ;
②用pH试纸测定图1中溶液的酸碱性:草木灰水pH>7,属于 (填“酸性”、“中性”或“碱性”)溶液,白醋pH 7;
③图2是三位同学分别测定某溶液酸碱性的操作示意图,其中正确的是 (填“A”、“B”或“C”,下同),可能导致被测溶液pH发生改变的错误操作是 .
为了证明长期暴露在空气中的氢氧化钠溶液已经变质,请分别选用二种不同物质类别的试剂完成二种实验方案的设计,并填写下列表格.
| 实验方案 | 选用试剂 | 涉及到的化学方程式 |
| 方案一 | 稀盐酸 |
|
| 方案二 | 氯化钙溶液 |
|
 过量
过量
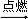 C+2MgO,以下说法错误的是( )
C+2MgO,以下说法错误的是( )