题目内容
通过化学知识的学习,我们已经能用化学知识解决一些实际问题.
(1)写出下列有关反应的化学方程式:胃酸(HCl)过多的人可以服用含Mg(OH)2的药物 ;用稀硫酸除去铁钉上的铁锈 .
(2)在酸碱中和实验中,由于未滴加酸碱指示剂,向盐酸中滴加氢氧化钠溶液,氢氧化钠溶液的滴加量不足,为证明盐酸有剩余,可选用下列试剂中的 .
A、铁粉 B、铜粉 C、AgNO3溶液 D、Na2CO3溶液.
(1)写出下列有关反应的化学方程式:胃酸(HCl)过多的人可以服用含Mg(OH)2的药物
(2)在酸碱中和实验中,由于未滴加酸碱指示剂,向盐酸中滴加氢氧化钠溶液,氢氧化钠溶液的滴加量不足,为证明盐酸有剩余,可选用下列试剂中的
A、铁粉 B、铜粉 C、AgNO3溶液 D、Na2CO3溶液.
考点:酸的化学性质,书写化学方程式、文字表达式、电离方程式
专题:常见的酸 酸的通性
分析:(1)首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.
(2)根据酸的化学性质进行分析解答即可.
(2)根据酸的化学性质进行分析解答即可.
解答:解:
(1)氢氧化镁与盐酸反应生成氯化镁和水,反应的化学方程式为:Mg(OH)2+2HCl═MgCl2+2H2O.
铁锈的主要成分是氧化铁,与硫酸反应生成硫酸铁和水,反应的化学方程式是为Fe2O3+3H2SO4=Fe2(SO4)3+3H2O.
(2)
A、铁的活动性比氢强,能与盐酸反应生成氢气,根据是否产生气泡,能用于检验盐酸过量,故选项正确.
B、AgNO3溶液与生成 的氯化钠溶液、盐酸均能反应生成氯化银白色沉淀,不能用于检验盐酸过量,故选项错误.
C、铜粉活动性比氢弱,不能与盐酸反应,不能用于检验盐酸过量,故选项错误.
D、Na2CO3溶液与盐酸反应生成二氧化碳气体,根据是否产生气泡,能用于检验盐酸过量,故选项正确.
故答案为:
(1)Mg(OH)2+2HCl═MgCl2+2H2O;Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;(2)AD.
(1)氢氧化镁与盐酸反应生成氯化镁和水,反应的化学方程式为:Mg(OH)2+2HCl═MgCl2+2H2O.
铁锈的主要成分是氧化铁,与硫酸反应生成硫酸铁和水,反应的化学方程式是为Fe2O3+3H2SO4=Fe2(SO4)3+3H2O.
(2)
A、铁的活动性比氢强,能与盐酸反应生成氢气,根据是否产生气泡,能用于检验盐酸过量,故选项正确.
B、AgNO3溶液与生成 的氯化钠溶液、盐酸均能反应生成氯化银白色沉淀,不能用于检验盐酸过量,故选项错误.
C、铜粉活动性比氢弱,不能与盐酸反应,不能用于检验盐酸过量,故选项错误.
D、Na2CO3溶液与盐酸反应生成二氧化碳气体,根据是否产生气泡,能用于检验盐酸过量,故选项正确.
故答案为:
(1)Mg(OH)2+2HCl═MgCl2+2H2O;Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;(2)AD.
点评:本题难度不大,掌握化学方程式的书写方法、酸的化学性质是正确解答本题的关键.

练习册系列答案
相关题目
 探究实验室中久置的NaOH的变质程度
探究实验室中久置的NaOH的变质程度
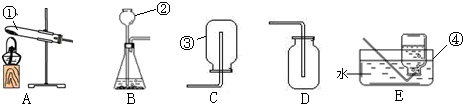
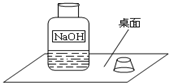 一天,实验助手小娟走进实验室,和老师一起检查每个实验桌上的药品、仪器是否齐备,走到某组的时候,看到了一个不和谐的“音符”(如图).
一天,实验助手小娟走进实验室,和老师一起检查每个实验桌上的药品、仪器是否齐备,走到某组的时候,看到了一个不和谐的“音符”(如图).