题目内容
4.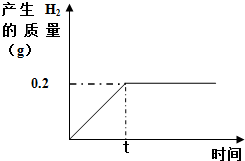 取一定质量的铁粉与100g稀硫酸反应,铁粉与稀硫酸恰好完全反应.产生的氢气随时间的变化如图所示:
取一定质量的铁粉与100g稀硫酸反应,铁粉与稀硫酸恰好完全反应.产生的氢气随时间的变化如图所示:求:(1)该反应一共生成氢气0.2g.
(2)参加反应的铁粉的质量5.6g.
(3)反应后所得溶液的溶质质量分数是多少?
分析 根据铁和稀硫酸反应生成硫酸亚铁和氢气,然后结合题中的数据进行解答.
解答 解:根据图可知:该反应一共生成氢气0.2g.
设参加反应的铁粉的质量为x,反应后所得溶液的溶质的质量为y,
Fe+H2SO4═FeSO4+H2↑
56 152 2
x y 0.2g
则$\frac{56}{2}=\frac{x}{0.2g}$,$\frac{152}{2}=\frac{y}{0.2g}$,解得x=5.6g,y=15.2g.
故反应后所得溶液的溶质质量分数是$\frac{15.2g}{100g+5.6g-0.2g}$×100%≈14.4%.
故答案为:
(1)0.2g;(2)5.6g;(3)14.4%.
点评 本题主要考查学生对有关化学方程式的计算能力.学生需正确书写出化学方程式,并能正确运用反应物与生成物间的质量关系进行计算,才能正确答题.

练习册系列答案
 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案
相关题目
14.用数轴表示某化学知识直观、简明、易记.下列用数轴表示的化学知识,错误的是( )
| A. | 部分元素原子序数关系: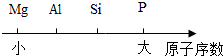 | |
| B. |  生活中常见物质的pH(常温下,中性溶液的pH为7,酸性溶液的pH<7,碱性溶液的pH>7): 生活中常见物质的pH(常温下,中性溶液的pH为7,酸性溶液的pH<7,碱性溶液的pH>7): | |
| C. | 地壳中部分元素的含量关系: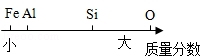 | |
| D. | 空气中部分成分的体积分数关系: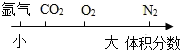 |
15.某同学将镁和金属X的混合物共2.4g加入足量的稀硫酸,充分反应后得到0.22gH2,则金属X可能是( )
| A. | Cu | B. | Zn | C. | Fe | D. | A1 |
12.分类是化学研究常用的方法.下列对物质分类正确的是( )
| A. | 过氧化钠(H2O2)和氧化钙(CaO)都属于氧化物 | |
| B. | 水和氢气都属于单质 | |
| C. | 碳酸钙(CaC03)和氢氧化钙(Ca(OH)2)都属于盐 | |
| D. | 火碱(NaOH)和碳酸钠(Na2CO3)都属于碱 |
9.除去CO2中的少量CO可行的方法是( )
| A. | 通入澄清石灰水 | B. | 倒掉 | ||
| C. | 燃烧 | D. | 通过灼热的氧化铜 |
13.下列实验方法不能达到实验目的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 区别烧碱和食盐 | 取固体加水,并测定溶液的温度 |
| B | 检验氧气是否收集满 | 将带火星的木条放在集气瓶口,观察是否复燃 |
| C | 区别羊毛和化纤布料 | 取样品燃烧,闻气味 |
| D | 除去CO2中混有的HCl气体 | 将气体通过NaOH溶液后再通过浓硫酸 |
| A. | A | B. | B | C. | C | D. | D |

 某兴趣小组在探究二氧化碳与氢氧化钠溶液反应的实验中,做了如图所示的实验:将足量的氢氧化钠弄溶液装入分液漏斗中,先打开阀门K1,待氢氧化钠溶液完全浸入广口瓶之后立即关闭K1,充分反应后,打开止水夹K2,请填写实验现象:
某兴趣小组在探究二氧化碳与氢氧化钠溶液反应的实验中,做了如图所示的实验:将足量的氢氧化钠弄溶液装入分液漏斗中,先打开阀门K1,待氢氧化钠溶液完全浸入广口瓶之后立即关闭K1,充分反应后,打开止水夹K2,请填写实验现象: